Hvorfor er faste stoffer og væsker kondenserede materialer?
Her er en sammenbrud:
* faste stoffer: I faste stoffer er molekylerne fastgjort i en stiv struktur med stærke intermolekylære kræfter, der holder dem sammen. Dette stramme arrangement fører til en fast form og volumen.
* væsker: I væsker er molekylerne også tæt pakket , men de har mere bevægelsesfrihed sammenlignet med faste stoffer. De kan glide forbi hinanden, hvilket resulterer i et fast volumen, men en variabel form.
I modsætning hertil gasser har meget svage intermolekylære kræfter, og deres molekyler er langt fra hinanden og bevæger sig tilfældigt . Dette gør det muligt for gasser at udvide til at fylde enhver beholder, de besætter.
Derfor betragtes både faste stoffer og væsker som kondenseret på grund af høj densitet af deres molekyler på grund af deres tæt pakning.
 Varme artikler
Varme artikler
-
 Nanokonstrueret cement viser løfte om tætning af utætte gasbrøndePå billedet ses en naturgasbrønd i Pennsylvania. Når brønde bliver beskadiget eller nedbrudt, metan kan potentielt slippe ud i miljøet. Penn State-forskere udviklede en ny nanomateriale-cementblanding
Nanokonstrueret cement viser løfte om tætning af utætte gasbrøndePå billedet ses en naturgasbrønd i Pennsylvania. Når brønde bliver beskadiget eller nedbrudt, metan kan potentielt slippe ud i miljøet. Penn State-forskere udviklede en ny nanomateriale-cementblanding -
 Bærbar gasdetektion krymper til nye dimensionerJoshua Whiting, en analytisk kemiker ved Sandia National Laboratories, undersøger en gassensor, der kunne bruges i et følsomt bærbart system til at opdage kemiske våben eller luftbårne toksiner. Kredi
Bærbar gasdetektion krymper til nye dimensionerJoshua Whiting, en analytisk kemiker ved Sandia National Laboratories, undersøger en gassensor, der kunne bruges i et følsomt bærbart system til at opdage kemiske våben eller luftbårne toksiner. Kredi -
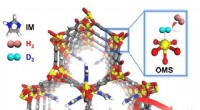 Udvikling af smart isotopadskillelsessystemMOF-74-IM. Kredit:UNIST Et internationalt team af forskere, tilknyttet UNIST har præsenteret et nyt hydrogenisotopseparationssystem baseret på et porøst metal organisk rammeværk (MOF). Isoleringen
Udvikling af smart isotopadskillelsessystemMOF-74-IM. Kredit:UNIST Et internationalt team af forskere, tilknyttet UNIST har præsenteret et nyt hydrogenisotopseparationssystem baseret på et porøst metal organisk rammeværk (MOF). Isoleringen -
 Brug af træ i elektroder for mere holdbarhed, bæredygtige wearablesNærbillede af træ og MXene komposit, med 40 procent træcellulose nanofibriller (CNF). Kredit:KTH Det Kongelige Tekniske Institut Træfibre er blevet brugt af forskere i Sverige til at skabe en ny k
Brug af træ i elektroder for mere holdbarhed, bæredygtige wearablesNærbillede af træ og MXene komposit, med 40 procent træcellulose nanofibriller (CNF). Kredit:KTH Det Kongelige Tekniske Institut Træfibre er blevet brugt af forskere i Sverige til at skabe en ny k


