Hvilken type materialer ville påvirke kuldioxid?
Materialer, der absorberer eller fjerner CO2:
* alkaliske løsninger:
* natriumhydroxid (NaOH) og kaliumhydroxid (KOH): Disse stærke baser reagerer med CO2 for at danne carbonater.
* Limewater (calciumhydroxid, CA (OH) 2): Reaktionen danner et hvidt bundfald af calciumcarbonat (CACO3), hvilket gør det til en god indikator for CO2 -tilstedeværelse.
* aminer (organiske forbindelser): Visse aminer, som monoethanolamin (MEA), bruges i industrielle processer til at fange CO2 fra røggasser.
* planter og alger: Fotosyntesen bruger CO2 som en kulstofkilde, omdanner den til sukker og frigiver ilt.
* oceaner: Oceans absorberer en betydelig mængde CO2 og danner kulsyre (H2CO3), hvilket påvirker havsyre.
* faste kulstofmaterialer:
* Aktivt kul: Dette porøse materiale kan adsorbere CO2.
* metalorganiske rammer (MOF'er): Disse meget porøse materialer med store overfladearealer undersøges for CO2 -indfangning og opbevaring.
Materialer, der frigiver CO2:
* forbrænding af brændstoffer: Brændende fossile brændstoffer som kul, olie og naturgas frigiver CO2 i atmosfæren.
* nedbrydning af organisk stof: Faldende plante- og dyrestof frigiver CO2 gennem mikrobielle processer.
* vulkansk aktivitet: Vulkaner frigiver CO2 fra Jordens interiør.
* Industrielle processer: Mange industrielle processer, såsom cementproduktion og stålproduktion, frigiver CO2 som et biprodukt.
Materialer, der reagerer med CO2 (men fjerner det ikke nødvendigvis):
* Metaller: Nogle metaller, som jern (Fe) og magnesium (Mg), kan reagere med CO2 for at danne oxider. Denne reaktion kan bruges i visse kemiske processer, men fjerner ikke permanent CO2.
* vand (H2O): CO2 opløses i vand og danner kulsyre (H2CO3), hvilket bidrager til forsuring af havet.
Vigtig note: Den måde, et materiale påvirker CO2, afhænger af dets specifikke egenskaber, de omgivende forhold (temperatur, tryk osv.) Og sammenhængen med interaktionen.
Fortæl mig, hvis du har flere spørgsmål!
 Varme artikler
Varme artikler
-
 Forskere skaber flydende frastødende stof, der virker på alle overfladerUBCO -masterstuderende Behrooz Khatir måler væske, der skal påføres en omnifobisk film under testning inde i OPERA -laboratoriet på UBC Okanagans Engineering School. Kredit:UBCO Handler som et usy
Forskere skaber flydende frastødende stof, der virker på alle overfladerUBCO -masterstuderende Behrooz Khatir måler væske, der skal påføres en omnifobisk film under testning inde i OPERA -laboratoriet på UBC Okanagans Engineering School. Kredit:UBCO Handler som et usy -
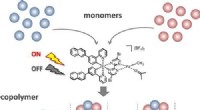 Brugerdefinerede sekvenser til polymerer ved hjælp af synligt lysBrugerdefineret sekvens af forskellige sammensætninger i en enkelt polymerkæde, skabt ved blot at udsætte en igangværende polymerisationsreaktion for forskellige tænd/sluk-sekvenser af synligt lys. Kr
Brugerdefinerede sekvenser til polymerer ved hjælp af synligt lysBrugerdefineret sekvens af forskellige sammensætninger i en enkelt polymerkæde, skabt ved blot at udsætte en igangværende polymerisationsreaktion for forskellige tænd/sluk-sekvenser af synligt lys. Kr -
 Syntese af nøgne aromatiske polymerer med dendrimerunderstøttelse gør det muligt at skabe unikke …Nøgne aromatiske polymerer syntetiseret af dendrimer-understøtning. Kredit:Issey Takahashi Bare aromatiske polymerer har potentiale til at blive brugt i en lang række højtydende og funktionelle mat
Syntese af nøgne aromatiske polymerer med dendrimerunderstøttelse gør det muligt at skabe unikke …Nøgne aromatiske polymerer syntetiseret af dendrimer-understøtning. Kredit:Issey Takahashi Bare aromatiske polymerer har potentiale til at blive brugt i en lang række højtydende og funktionelle mat -
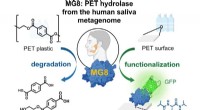 Enzym i menneskelige spytmikrober nedbryder PET-baseret plastKredit:Wiley Menneskespyt kan indeholde et enzym, som kan nedbryde plasten polyethylenterephthalat (PET). Forskere fandt det lovende enzym, en hydrolase, i en database, der indeholder prøver fra me
Enzym i menneskelige spytmikrober nedbryder PET-baseret plastKredit:Wiley Menneskespyt kan indeholde et enzym, som kan nedbryde plasten polyethylenterephthalat (PET). Forskere fandt det lovende enzym, en hydrolase, i en database, der indeholder prøver fra me


