Hvorfor har triethylaminvandssystem lavere konsoluttemperatur?
1. Hydrogenbinding:
* Vand: Vandmolekyler er meget polære og danner stærke brintbindinger med hinanden.
* triethylamin: Triethylamin er et ikke-polært molekyle og danner ikke brintbindinger med vand.
2. Entropi og entalpi:
* lave temperaturer: Ved lave temperaturer favoriseres entropiforstærkningen ved blanding. Dette betyder, at systemet favoriserer en mere forstyrret tilstand med begge komponenter opløst.
* Høje temperaturer: Efterhånden som temperaturen stiger, bliver entalpi -udtrykket mere dominerende. De ugunstige interaktioner mellem vand og triethylamin bliver mere udtalt, hvilket fører til faseseparation.
3. Hydrofobe effekter:
* Triethylamin er et hydrofobt molekyle, hvilket betyder, at det afviser vand. Ved højere temperaturer bliver den hydrofobe virkning stærkere, hvilket får triethylaminmolekylerne til at klynge sig sammen og adskille sig fra vandfasen.
4. Molekylær størrelse og form:
* Triethylamin er et relativt stort molekyle med en voluminøs struktur. Denne forskel i størrelse og form mellem triethylamin og vandmolekyler bidrager til de ugunstige interaktioner ved højere temperaturer.
Kortfattet:
Den lavere konsoluttemperatur i triethylamin-vand-systemet opstår fra samspillet mellem hydrogenbinding, entropi, entalpi, hydrofobe virkninger og forskelle i molekylær størrelse og form. Ved lave temperaturer opvejer entropiforøgelsen ved at blande sig de ugunstige interaktioner, hvilket fører til blanding. Efterhånden som temperaturen stiger, bliver de ugunstige interaktioner mere dominerende, hvilket resulterer i faseseparation og en lavere konsoluttemperatur.
 Varme artikler
Varme artikler
-
 Synkrotronundersøgelse afslører oxygens indflydelse på kemien af atmosfærisk forureningEt repræsentativt brændstofmolekyle, der viser iltmolekyler (højre, rød) og 2-methylheptan (højre, grå og hvid) mødes i en jet-omrørt reaktor. De stærkt oxygenerede molekyler, der resulterer (til vens
Synkrotronundersøgelse afslører oxygens indflydelse på kemien af atmosfærisk forureningEt repræsentativt brændstofmolekyle, der viser iltmolekyler (højre, rød) og 2-methylheptan (højre, grå og hvid) mødes i en jet-omrørt reaktor. De stærkt oxygenerede molekyler, der resulterer (til vens -
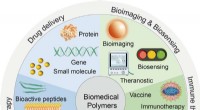 Biomedicinske polymerer:syntese, egenskaber og anvendelserSkematisk illustration af smarte polymerer til biomedicinske applikationer. Kredit:Science China Press Biomedicinske polymerer er blevet omfattende udviklet til lovende anvendelser inden for en mas
Biomedicinske polymerer:syntese, egenskaber og anvendelserSkematisk illustration af smarte polymerer til biomedicinske applikationer. Kredit:Science China Press Biomedicinske polymerer er blevet omfattende udviklet til lovende anvendelser inden for en mas -
 Strækbare superkondensatorer til at drive morgendagens bærbare enhederDisse skovlignende rækker af kulstofnanorør blev skabt på et elastomersubstrat, der blev forstrakt i én retning og derefter fik lov til at trække sig sammen. Denne proces skaber strækbare superkondens
Strækbare superkondensatorer til at drive morgendagens bærbare enhederDisse skovlignende rækker af kulstofnanorør blev skabt på et elastomersubstrat, der blev forstrakt i én retning og derefter fik lov til at trække sig sammen. Denne proces skaber strækbare superkondens -
 Vurdering af salens potentielle aktivitet mod proteiner af SARS-CoV-2Ifølge videnskabsmænd er salen - stoffet på billedet - relativt simpelt og billigt at syntetisere. Kredit:UrFU / Damir Safin Forskere fandt ud af, at salen effektivt er i stand til at binde en rækk
Vurdering af salens potentielle aktivitet mod proteiner af SARS-CoV-2Ifølge videnskabsmænd er salen - stoffet på billedet - relativt simpelt og billigt at syntetisere. Kredit:UrFU / Damir Safin Forskere fandt ud af, at salen effektivt er i stand til at binde en rækk
- Fakta om Cedar Trees
- At komme til hjertet af kortlægning af arytmi-relaterede excitationer
- Trump til at udvikle en national strategi for trådløse 5G -netværk
- Sundhedssektoren giver blockchain glødende prognose
- Undersøgelse af, hvordan gener aktiveres, giver overraskende opdagelser
- Dødstallet fra oversvømmelser i Venezuela stiger til otte


