Hvordan er overgangsmetaller forbindelser?
1. Variabel oxidation siger:
* Nøglefunktion: Overgangsmetaller har flere oxidationstilstande (positive ladninger), fordi de kan miste elektroner fra både deres ydre * s * og * d * orbitaler. Dette giver dem mulighed for at danne forbindelser med forskellige støkiometrier og egenskaber.
* Eksempel: Jern kan danne fe²⁺ (jernholdigt) og Fe³⁺ (ferrisk) ioner, hvilket fører til forbindelser som fecl₂ (jernløst chlorid) og fecl₃ (ferricchlorid).
2. Dannelse af farvede forbindelser:
* Nøglefunktion: Overgangsmetalioner har uparrede elektroner i deres * d * orbitaler, som kan absorbere specifikke bølgelængder af lys og genemitere andre, hvilket resulterer i livlige farver.
* Eksempel: Kobber (II) ioner (Cu²⁺) er blå på grund af absorptionen af rødt lys, mens mangan (VII) -ioner (Mno₄⁻) er lilla, fordi de absorberer grønt lys.
3. Kompleks iondannelse:
* Nøglefunktion: Overgangsmetaller danner let komplekse ioner ved at koordinere med ligander (molekyler eller ioner, der donerer elektronpar).
* Eksempel: Kobber (II) ion (Cu²⁺) kan danne den komplekse ion [Cu (H₂O) ₄] ²⁺ med vandmolekyler som ligander, hvilket giver den en karakteristisk blå farve i vandig opløsning.
4. Katalytisk aktivitet:
* Nøglefunktion: Overgangsmetaller og deres forbindelser fungerer ofte som katalysatorer og fremskynder kemiske reaktioner uden at blive konsumeret i processen.
* Eksempel: Nikkel bruges som en katalysator i hydrogenering af vegetabilske olier til at producere margarine.
5. Magnetiske egenskaber:
* Nøglefunktion: Tilstedeværelsen af uparrede elektroner i * d * orbitaler kan føre til paramagnetisme (tiltrækning til magnetiske felter) eller ferromagnetisme (stærk tiltrækning til magnetiske felter).
* Eksempel: Jern (Fe) udviser ferromagnetisme og er grundlaget for permanente magneter.
Eksempler på overgangsmetalforbindelser:
* Oxider: Jernoxid (Fe₂o₃) findes i rust og bruges som et pigment.
* sulfider: Zinksulfid (ZnS) bruges i fluorescerende lys.
* halogenider: Kobber (II) Chlorid (Cucl₂) er et grønt fast stof, der bruges som et pigment.
* carbonylkomplekser: Nikkel tetracarbonyl (Ni (CO) ₄) er en meget giftig og flygtig forbindelse, der anvendes til oprensning af nikkel.
Kortfattet:
Overgangsmetaller danner en bred vifte af forbindelser på grund af deres evne til at udvise flere oxidationstilstande, danne komplekse ioner og udvise katalytiske og magnetiske egenskaber. Deres forbindelser er vigtige for forskellige teknologier, fra pigmenter og katalysatorer til batterier og magneter.
Sidste artikelGiv dig 10 eksempler på solid?
Næste artikelHvad er produkterne fra forbrænding af 2-methyl- og 3-ethyloctan?
 Varme artikler
Varme artikler
-
 Kalium giver perovskit-baserede solceller et effektivitetsløftAtomisk skala billede af perovskit krystal struktur dannelse (selvsamlende). Kaliumionerne (i rødt) dekorerer overfladerne af strukturerne for at helbrede defekter og immobiliserer de overskydende hal
Kalium giver perovskit-baserede solceller et effektivitetsløftAtomisk skala billede af perovskit krystal struktur dannelse (selvsamlende). Kaliumionerne (i rødt) dekorerer overfladerne af strukturerne for at helbrede defekter og immobiliserer de overskydende hal -
 Et nyt værktøj til styring af reaktioner i mikrorobotter og mikroreaktorerThomas Russell og Ganhua Xie ved UMass Amherst og Lawrence Berkeley National Lab bruger kapillære kræfter til at udvikle en simpel metode til fremstilling af selvsamlende hængende dråber af en vandig
Et nyt værktøj til styring af reaktioner i mikrorobotter og mikroreaktorerThomas Russell og Ganhua Xie ved UMass Amherst og Lawrence Berkeley National Lab bruger kapillære kræfter til at udvikle en simpel metode til fremstilling af selvsamlende hængende dråber af en vandig -
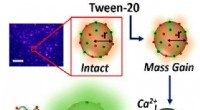 Forskere afslører, hvordan vaskemidler faktisk virkerGrafisk abstrakt. Kredit:The Journal of Physical Chemistry Letters (2022). DOI:10.1021/acs.jpclett.2c00704 Forskere har opdaget den præcise måde, hvorpå rengøringsmidler bryder biologiske membraner
Forskere afslører, hvordan vaskemidler faktisk virkerGrafisk abstrakt. Kredit:The Journal of Physical Chemistry Letters (2022). DOI:10.1021/acs.jpclett.2c00704 Forskere har opdaget den præcise måde, hvorpå rengøringsmidler bryder biologiske membraner -
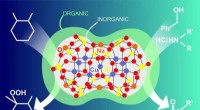 Kemikere syntetiserer en ny hybrid organisk-uorganisk katalysatorKredit:Natalia Deryugina RUDN -kemikere har syntetiseret metalkomplekser på basis af det organoelementale stof silsesquioxan, der består af en organisk og en uorganisk del. Sådanne hybridsystemer
Kemikere syntetiserer en ny hybrid organisk-uorganisk katalysatorKredit:Natalia Deryugina RUDN -kemikere har syntetiseret metalkomplekser på basis af det organoelementale stof silsesquioxan, der består af en organisk og en uorganisk del. Sådanne hybridsystemer
- Hvad gør et prisme med hvidt lys?
- Triboelektriske nanogeneratorer øger massespektrometriydelsen
- Hvad er eksempler på gennemsigtige materialer?
- En unik kombination af katalysatorer åbner døre til fremstilling af nyttige forbindelser
- To nye oppustede varme Jupitere opdaget af astronomer
- Virkningen af COVID-19 har skabt store uoverensstemmelser i elevernes erfaringer med at tage A-niv…


