Når et metalatom kombineres med ikke-metal, hvordan vil reaktionen?
1. Elektronoverførsel:
* metalatomer har en tendens til at miste elektroner for at opnå en stabil elektronkonfiguration (som en ædel gas). De bliver positivt ladede ioner (kationer).
* ikke-metalatomer har en tendens til at få elektroner for at opnå en stabil elektronkonfiguration. De bliver negativt ladede ioner (Anioner).
2. Elektrostatisk tiltrækning:
* De modsatte ladede ioner tiltrækkes af hinanden på grund af elektrostatiske kræfter. Denne attraktion danner en stærk ionisk binding .
3. Dannelse af en forbindelse:
* Ionerne arrangerer sig selv i et specifikt, gentagne mønster kaldet A krystalgitter For at maksimere elektrostatisk tiltrækning.
* Den resulterende forbindelse er generelt neutral, da de positive og negative afgifter afbalanceres.
Eksempel:
* natrium (NA) , et metal, mister et elektron for at blive en natriumion (Na⁺).
* klor (Cl) , en ikke-metal, får et elektron til at blive en chloridion (CL⁻).
* Disse ioner tiltrækker hinanden og danner natriumchlorid (NaCl), almindeligvis kendt som bordsalt.
Nøgleegenskaber for ioniske forbindelser:
* høje smelte- og kogepunkter På grund af stærk elektrostatisk tiltrækning.
* sprød Fordi ionerne er tæt pakket, og enhver forstyrrelse forstyrrer gitterstrukturen.
* Led elektricitet, når den er smeltet eller opløst i vand Fordi ionerne bliver frie til at bevæge sig.
* generelt opløselig i vand Fordi vandmolekyler kan omringe og adskille ionerne.
Fortæl mig, hvis du vil gå dybere ned i specifikke eksempler eller andre aspekter af ionisk binding!
 Varme artikler
Varme artikler
-
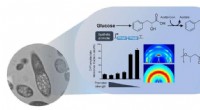 Et-trins produktion af aromatiske polyestere af E. coli-stammerBiosyntese af aromatiske polyestere ved metabolisk manipuleret E coli .Dette skematiske diagram viser den overordnede konceptualisering af, hvordan metabolisk manipuleret E coli fremstillet aromat
Et-trins produktion af aromatiske polyestere af E. coli-stammerBiosyntese af aromatiske polyestere ved metabolisk manipuleret E coli .Dette skematiske diagram viser den overordnede konceptualisering af, hvordan metabolisk manipuleret E coli fremstillet aromat -
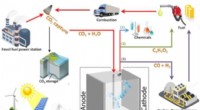 Forskere laver alkohol ud af den blå luftTre forskellige måder, hvorpå elektroreduktion af CO2 potentielt kan lukke kulstofkredsløbet. Kredit:Delft University of Technology Det lyder måske for godt til at være sandt, men TU Delft-ph.d.-s
Forskere laver alkohol ud af den blå luftTre forskellige måder, hvorpå elektroreduktion af CO2 potentielt kan lukke kulstofkredsløbet. Kredit:Delft University of Technology Det lyder måske for godt til at være sandt, men TU Delft-ph.d.-s -
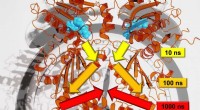 Forskere undersøger signaloverførsel i proteiner på tværs af flere tidsskalaerForskere fra Freiburg har været i stand til at analysere den præcise signaloverførselshastighed på tværs af flere tidsskalaer. Kredit:Steffen Wolf Overvej et øjeblik et træ, der svajer i vinden. H
Forskere undersøger signaloverførsel i proteiner på tværs af flere tidsskalaerForskere fra Freiburg har været i stand til at analysere den præcise signaloverførselshastighed på tværs af flere tidsskalaer. Kredit:Steffen Wolf Overvej et øjeblik et træ, der svajer i vinden. H -
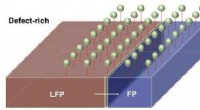 Forskere viser punktdefekter i katodekrystaller kan fremskynde lithiumabsorptionEn illustration viser et batteris katode, der gennemgår faseovergang fra jernfosfat (FP) til lithiumjernfosfat (LFP) under opladning. Simuleringer fra Rice University-forskere viste, at tilføjelse af
Forskere viser punktdefekter i katodekrystaller kan fremskynde lithiumabsorptionEn illustration viser et batteris katode, der gennemgår faseovergang fra jernfosfat (FP) til lithiumjernfosfat (LFP) under opladning. Simuleringer fra Rice University-forskere viste, at tilføjelse af
- Forvandle dødelige fjender til allierede? Myrer kan
- Magnetiske mikrorobotter bruger kapillarkræfter til at lokke partikler til position
- Brug af molekylære simuleringer til at studere selvsamlende associerende polymerer
- Hvilken type stjerne ville følge Path Stars Evolution?
- Sådan finder du spænding og strøm over en kreds i serie & i Parallel
- Hvordan fjernes malme under jordoverfladen?


