Hvad hjælper med at bestemme, om en løsning er syre eller grundlæggende?
1. pH -skala
* PH -skalaen varierer fra 0 til 14, med:
* 0-6: Sur
* 7: Neutral (som rent vand)
* 8-14: Grundlæggende (også kaldet alkalisk)
* måling af pH:
* lakmuspapir: Bliv røde i sure opløsninger, blå i basale opløsninger.
* pH -meter: Giver en numerisk læsning af pH.
* indikatorer: Visse kemikalier ændrer farve afhængigt af pH.
2. Tilstedeværelsen af ioner
* syrer Slip hydrogenioner (H+), når det blev opløst i vand.
* baser Slip hydroxidioner (OH-), når det opløses i vand.
* neutrale løsninger har omtrent lige store mængder H+ og OH-.
3. Andre egenskaber
* syrer: Smag ofte surt, reagerer med metaller for at producere brintgas og kan dreje blåt lakmuspapir rød.
* baser: Smag ofte bitter, føl dig glat og kan blive rød lakmuspapirblå.
nøglekoncepter
* stærke syrer og baser: Ioniser sig fuldstændigt i vand, hvilket betyder, at de frigiver alle deres H+ eller OH-ioner.
* svage syrer og baser: Delvis ionisere i vand.
Eksempel:
* eddike er sur, fordi den indeholder eddikesyre, der frigiver H+ -ioner, når de opløses i vand.
* bagepulver er basisk, fordi det indeholder natriumbicarbonat, der frigiver ohioner, når de opløses i vand.
Lad mig vide, om du vil udforske specifikke eksempler eller har brug for yderligere forklaring!
 Varme artikler
Varme artikler
-
 Beregningsanalyse afslører den komplekse adfærd af en polymerFigur 1:Konventionelle plastmaterialer som f.eks. Disse plasticchips fra genanvendte vandflasker er vanskelige at nedbryde i deres monomer byggesten. Nu, RIKEN -forskere har afsløret den komplekse dep
Beregningsanalyse afslører den komplekse adfærd af en polymerFigur 1:Konventionelle plastmaterialer som f.eks. Disse plasticchips fra genanvendte vandflasker er vanskelige at nedbryde i deres monomer byggesten. Nu, RIKEN -forskere har afsløret den komplekse dep -
 Returnering af nitrogen til jord uden kemikalierKredit:Flinders University Mens landbrugsproduktionen rundt om i verden kæmper med faldende jordsundhed, Australske forskere undersøger produktionen af en bæredygtig organisk nitrogengødning fre
Returnering af nitrogen til jord uden kemikalierKredit:Flinders University Mens landbrugsproduktionen rundt om i verden kæmper med faldende jordsundhed, Australske forskere undersøger produktionen af en bæredygtig organisk nitrogengødning fre -
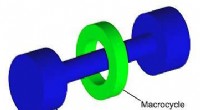 Forskere laver verdens hurtigste molekylære skytteSkematisk fremstilling af en rotaxan, den type molekyle, der var genstand for undersøgelsen. Kredit:Wikimedia Commons Takket være et smart kemisk design, Det er lykkedes forskere ved universitetet
Forskere laver verdens hurtigste molekylære skytteSkematisk fremstilling af en rotaxan, den type molekyle, der var genstand for undersøgelsen. Kredit:Wikimedia Commons Takket være et smart kemisk design, Det er lykkedes forskere ved universitetet -
 Er antivitaminer det nye antibiotika?Kredit:CC0 Public Domain Antibiotika er blandt de vigtigste opdagelser af moderne medicin og har reddet millioner af liv siden opdagelsen af penicillin for næsten 100 år siden. Mange sygdomme fo
Er antivitaminer det nye antibiotika?Kredit:CC0 Public Domain Antibiotika er blandt de vigtigste opdagelser af moderne medicin og har reddet millioner af liv siden opdagelsen af penicillin for næsten 100 år siden. Mange sygdomme fo
- Hvis en genstand har en masse på 85 g og volumen 92 cm 3, hvad er dens massefylde?
- ATLAS frigiver første måling af W -masse ved hjælp af LHC -data
- Merkel:1 million billadestationer i Tyskland inden 2030
- "Megalodon Facts for Kids
- Anti-degranulering og galdesyrebindende aktivitet af frugter og agroindustrielle biprodukter
- Lysende nanoserede krystaller viser løfte om at kigge dybt ind i kropsvæv


