En beholder er fyldt med 4,0 x 1022 O2 -molekyler ved 5 grader celsius og 845 mm Hg Hvad volumen i ml container?
1. Konverter enheder
* temperatur (t): 5 grader Celsius til Kelvin:5 + 273,15 =278,15 K
* tryk (p): 845 mm Hg til atmosfærer (ATM):845 mm Hg / 760 mm Hg / atm =1.112 atm
* antal molekyler (n): Til mol (n):4,0 x 10^22 molekyler / 6,022 x 10^23 molekyler / mol =0,0665 mol
2. Ideel gaslov
Den ideelle gaslov er:PV =NRT
Hvor:
* P =pres (i ATM)
* V =volumen (i liter)
* n =antal mol
* R =ideel gaskonstant (0,0821 l · atm/mol · k)
* T =temperatur (i Kelvin)
3. Løs for volumen (v)
Omarranger den ideelle gaslov til at løse for V:
V =(nrt) / p
4. Beregn
V =(0,0665 mol * 0,0821 L · ATM / Mol · K * 278,15 K) / 1.112 ATM
V ≈ 1,37 L
5. Konverter til ML
V ≈ 1,37 L * 1000 ml/L ≈ 1370 ml
Derfor er beholderens volumen ca. 1370 ml
 Varme artikler
Varme artikler
-
 Enzymopdagelse kan hjælpe med at bekæmpe tuberkuloseKredit:University of Warwick En enzymstruktur opdagelse foretaget af forskere ved University of Warwick kan hjælpe med at udrydde tuberkulose (TB). Forskning udført af et hold ledet af Dr. Elizab
Enzymopdagelse kan hjælpe med at bekæmpe tuberkuloseKredit:University of Warwick En enzymstruktur opdagelse foretaget af forskere ved University of Warwick kan hjælpe med at udrydde tuberkulose (TB). Forskning udført af et hold ledet af Dr. Elizab -
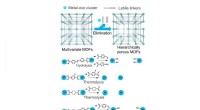 Strategier til at generere større porer i metal-organiske rammerIntroduktion af mesoporer i mikroporøse multivariate MOFer ved selektivt at fjerne labile linkere gennem hydrolyse, termolyse og ozonolyse. Gengivet fra Chem. Soc. Rev., 2019, 48, 4823-4853 med tillad
Strategier til at generere større porer i metal-organiske rammerIntroduktion af mesoporer i mikroporøse multivariate MOFer ved selektivt at fjerne labile linkere gennem hydrolyse, termolyse og ozonolyse. Gengivet fra Chem. Soc. Rev., 2019, 48, 4823-4853 med tillad -
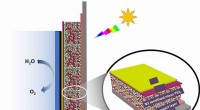 Lille titaniumbarriere stopper stort problem i brændstofproducerende solcellerIndkapsling af molekylkomponenterne i en solid-state farvestof-sensibiliseret solcelle ved en tynd tunnelspærre forbedrer dramatisk cellestabiliteten under vandspaltningsforhold (H2O til O2). Kredit:U
Lille titaniumbarriere stopper stort problem i brændstofproducerende solcellerIndkapsling af molekylkomponenterne i en solid-state farvestof-sensibiliseret solcelle ved en tynd tunnelspærre forbedrer dramatisk cellestabiliteten under vandspaltningsforhold (H2O til O2). Kredit:U -
 Strontium-iridiumoxid bruges til tilpasning som elektronisk materialeThorsten Schmitt (til venstre) og Milan Radovic på deres forsøgsstation ved Swiss Light Source SLS, hvor de udførte deres målinger på tynde film af strontium-iridiumoxid. Kredit:Paul Scherrer Institut
Strontium-iridiumoxid bruges til tilpasning som elektronisk materialeThorsten Schmitt (til venstre) og Milan Radovic på deres forsøgsstation ved Swiss Light Source SLS, hvor de udførte deres målinger på tynde film af strontium-iridiumoxid. Kredit:Paul Scherrer Institut
- Ny sensor registrerer værdifuldt sjældent jordelement terbium fra utraditionelle kilder
- Hvordan lærer man et folkeskolebarn om samtykke? Du kan starte med disse bøger
- Stillehavsøerne kan ikke tackle klimaændringer alene:Verdensbanken
- Hvorfor er Nucleus Call Celler -biblioteket?
- Hvad er radial spaltning?
- Ababis og Star Wnrs:Knockoffs trives i Kinas e-handel


