Hvem af følgende er klassificeret som en elektrongruppe?
Elektrongrupper
En elektrongruppe henviser til ethvert område omkring et centralt atom, hvor elektroner er koncentreret. Dette inkluderer:
* Ensomme par: Par elektroner, der ikke er involveret i binding.
* enkelt obligationer: Et par elektroner delte mellem to atomer.
* dobbeltobligationer: To par elektroner delte mellem to atomer.
* Triple Bonds: Tre par elektroner delte mellem to atomer.
Eksempel:
Lad os sige, at vi har molekylvandet (H₂O). Det centrale atom er ilt.
* Oxygen har to ensomme par.
* Oxygen danner to enkeltbindinger med brintatomer.
Derfor har vand i alt fire elektrongrupper omkring iltatomet (to ensomme par + to enkeltbindinger).
Vigtig note: VSEPR -teorien fokuserer på arrangementet af elektrongrupper omkring et centralt atom for at forudsige formen på et molekyle.
for at besvare dit spørgsmål:
Du skal give mig en liste over indstillinger for at bestemme, hvilke der er klassificeret som elektrongrupper. For eksempel kan du give en liste over ting som:
* Enkelt obligation
* Ensom par
* Dobbelt obligation
* Carbonatom
* Hydrogenatom
Jeg kan derefter fortælle dig, hvilke af dem der er elektrongrupper.
Sidste artikelHvilket flydende metal bruges mest i termometer?
Næste artikelAtomer har 2 dele, hvad er de, og hvordan er hver enkelt ladet?
 Varme artikler
Varme artikler
-
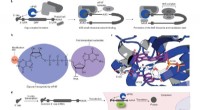 Biokemikere bruger nyt værktøj til at kontrollere mRNA ved hjælp af lys5′-hætten er et kendetegn for eukaryote mRNAer, der styrer translationsinitiering. a, Nøgletrin i oversættelsesinitiering. Den eukaryote translationsinitieringsfaktor eIF4E binder direkte til 5′-hætte
Biokemikere bruger nyt værktøj til at kontrollere mRNA ved hjælp af lys5′-hætten er et kendetegn for eukaryote mRNAer, der styrer translationsinitiering. a, Nøgletrin i oversættelsesinitiering. Den eukaryote translationsinitieringsfaktor eIF4E binder direkte til 5′-hætte -
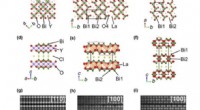 Teambilledressourcer brugt i internationalt eksperiment med nye fotokatalysatorerKredit:Skolkovo Institut for Videnskab og Teknologi Skoltech-forskere hjalp deres kolleger fra Japan, Tyskland, De Forenede Stater, og Kina studerer krystalstrukturen og optiske egenskaber af en n
Teambilledressourcer brugt i internationalt eksperiment med nye fotokatalysatorerKredit:Skolkovo Institut for Videnskab og Teknologi Skoltech-forskere hjalp deres kolleger fra Japan, Tyskland, De Forenede Stater, og Kina studerer krystalstrukturen og optiske egenskaber af en n -
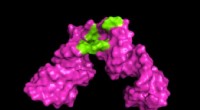 Forskere udvikler værktøjer til at skærpe 3D-visning af store RNA-molekylerUniversity of Maryland forskere udviklede en metode til at udvide omfanget af nuklear magnetisk resonans (NMR) spektroskopi. I eksemplet ovenfor, forskerne var i stand til at skabe et 3D-billede, der
Forskere udvikler værktøjer til at skærpe 3D-visning af store RNA-molekylerUniversity of Maryland forskere udviklede en metode til at udvide omfanget af nuklear magnetisk resonans (NMR) spektroskopi. I eksemplet ovenfor, forskerne var i stand til at skabe et 3D-billede, der -
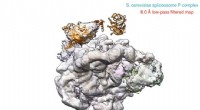 Spliceosomet - nu tilgængeligt i high definitionUCLA-forskere har løst strukturen i høj opløsning i en massiv mobilmaskine, spliceosome, udfylde det sidste store hul i vores forståelse af RNA -splejsningsprocessen, der tidligere var uklar. Kryo -e
Spliceosomet - nu tilgængeligt i high definitionUCLA-forskere har løst strukturen i høj opløsning i en massiv mobilmaskine, spliceosome, udfylde det sidste store hul i vores forståelse af RNA -splejsningsprocessen, der tidligere var uklar. Kryo -e


