Når elementer danner forbindelser, hvad gør gøren?
Hvad sker der:
* Deling eller overførsel af elektroner: Den grundlæggende ændring er deling eller overførsel af elektroner mellem elementernes atomer.
* stabilitet: Atomer forsøger at opnå en stabil elektronkonfiguration, der normalt ligner de ædle gasser, der har fulde ydre skaller.
* nyt stof: Den resulterende forbindelse har helt forskellige egenskaber end de originale elementer. Tænk på vand (H₂O) - Det er meget anderledes end brintgas (H₂) og iltgas (O₂).
Typer af kemisk binding:
* ionisk binding: Et atom (normalt et metal) mister elektroner og bliver en positivt ladet ion (kation), og et andet atom (normalt en ikke -metal) får disse elektroner og bliver en negativt ladet ion (anion). Disse modsatte ladede ioner tiltrækkes derefter af hinanden og danner den ioniske forbindelse.
* kovalent binding: To eller flere ikke -metale atomer deler elektroner for at opnå en stabil ydre skal. Dette resulterer i et molekyle.
Eksempler:
* natriumchlorid (NaCl) - ionisk binding: Natrium (NA) mister et elektron for at blive Na+, mens klor (CL) får et elektron til at blive Cl-. De resulterende ioner tiltrækker og danner natriumchlorid, et bordsalt.
* vand (H₂O) - Kovalent binding: To hydrogenatomer deler hver et elektron med et iltatom, der danner kovalente bindinger.
I resumé, når elementer danner forbindelser, binder de kemisk ved at dele eller overføre elektroner for at opnå stabilitet. Dette resulterer i et nyt stof med helt forskellige egenskaber.
Sidste artikelHvad bruges især fluorulfurinsyre til?
Næste artikelHvad er de fem agenter for kemisk forvitring?
 Varme artikler
Varme artikler
-
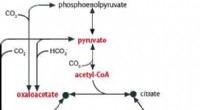 Opdagelse af et oprindeligt metabolisk system, der giver os et glimt af livets oprindelse på JordenFig. 1:Forholdet mellem TCA -cyklussen og pyruvat, acetyl-CoA, oxaloacetat, oxoglutarat, og succinyl-CoA er vist. Kredit:Hokkaido University Multi-omics forskning på Thermosulfidibacter (isoleret
Opdagelse af et oprindeligt metabolisk system, der giver os et glimt af livets oprindelse på JordenFig. 1:Forholdet mellem TCA -cyklussen og pyruvat, acetyl-CoA, oxaloacetat, oxoglutarat, og succinyl-CoA er vist. Kredit:Hokkaido University Multi-omics forskning på Thermosulfidibacter (isoleret -
 Forskere designer organisk katode til højtydende batterierHovedforfatter Zulipiya Shadike (til højre) er afbilledet ved NSLS-IIs XPD-strålelinje sammen med videnskabsmand og medforfatter Sanjit Ghose (til venstre). Kredit:Brookhaven National Laboratory F
Forskere designer organisk katode til højtydende batterierHovedforfatter Zulipiya Shadike (til højre) er afbilledet ved NSLS-IIs XPD-strålelinje sammen med videnskabsmand og medforfatter Sanjit Ghose (til venstre). Kredit:Brookhaven National Laboratory F -
 Særligt blåt lys – forsker finder ud af, at nye kemiske klynger udsender meget effektivt lysKredit:Wiley Et forskningshold fra Florida State University har opdaget, at en unik organisk-uorganisk forbindelse, der indeholder nul-dimensionelle molekylære klynger, udsender et meget effektivt
Særligt blåt lys – forsker finder ud af, at nye kemiske klynger udsender meget effektivt lysKredit:Wiley Et forskningshold fra Florida State University har opdaget, at en unik organisk-uorganisk forbindelse, der indeholder nul-dimensionelle molekylære klynger, udsender et meget effektivt -
 Farveskiftende bandager fornemmer og behandler bakterielle infektionerEn bandage ændrede farve fra grøn til gul, og fra grønt til rødt, i nærvær af stigende koncentrationer af lægemiddelfølsomme (DS) og lægemiddelresistente (DR) E coli , henholdsvis. Kredit:Tilpasset
Farveskiftende bandager fornemmer og behandler bakterielle infektionerEn bandage ændrede farve fra grøn til gul, og fra grønt til rødt, i nærvær af stigende koncentrationer af lægemiddelfølsomme (DS) og lægemiddelresistente (DR) E coli , henholdsvis. Kredit:Tilpasset
- Hvilke væsker sælges af gallonen?
- Forbedring af fremtidens oprensning ved at bruge molekylær silhuet til at adskille forbindelser i v…
- Cichlidefiskes nysgerrighed fremmer biodiversitet:Hvordan udforskende adfærd hjælper med økologis…
- Forskere søger en måde at gøre solceller ultratynde, fleksibel
- Hvilke ioner er det begrænsende reagens, og hvilket overskud, når bariumsulfat lavede?
- King of Swords:Optrævler den intellektuelle herskers hemmeligheder


