Linjemissionsspektret af et atom er forårsaget af energierne frigivet, når elektroner?
Her er en sammenbrud:
* Elektroner i atomer: Elektroner i atomer findes i specifikke energiniveauer. Disse niveauer er kvantiseret, hvilket betyder, at elektroner kun kan optage visse diskrete energiforhold.
* ophidset tilstand: Når en elektron absorberer energi (fra varme, lys eller andre kilder), springer det til et højere energiniveau og bliver "ophidset."
* Afslapning og emission: Den ophidsede tilstand er ustabil. Elektronet vender til sidst tilbage til et lavere energiniveau og frigiver den absorberede energi som en foton af lys.
* linjespektrum: Da energiniveauet er kvantiseret, er energiforskellene mellem dem specifikke. Dette resulterer i, at fotoner med specifikke bølgelængder udsendes, hvilket skaber de forskellige linjer i emissionsspektret.
Key Takeaway: Linjemissionsspektre er et unikt fingeraftryk af et element, der afslører de specifikke energiniveauovergange, der forekommer inden for dets atomer.
Sidste artikelHvilke planeter lavet af gas?
Næste artikelAf hvilket stof er de ydre planeter for det meste sammensat?
 Varme artikler
Varme artikler
-
 Ny polymer fremstillingsproces sparer 10 størrelsesordener af energiUniversity of Illinois forskere Philippe Geubelle, venstre, Scott White, Nancy Sottos og Jeffrey Moore har udviklet en ny polymerhærdningsproces, der kan reducere mængden af tid og energi, der forbr
Ny polymer fremstillingsproces sparer 10 størrelsesordener af energiUniversity of Illinois forskere Philippe Geubelle, venstre, Scott White, Nancy Sottos og Jeffrey Moore har udviklet en ny polymerhærdningsproces, der kan reducere mængden af tid og energi, der forbr -
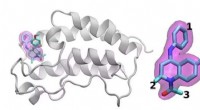 Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid
Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid -
 Cementfri beton slår korrosion og giver fatbergs skylEt fatberg udstillet i Melbourne Museum. Kredit:Copyright Museums Victoria, Fotograf:Rob Zugaro Forskere fra RMIT University har udviklet en miljøvenlig nul-cementbeton, hvilket næsten eliminerer
Cementfri beton slår korrosion og giver fatbergs skylEt fatberg udstillet i Melbourne Museum. Kredit:Copyright Museums Victoria, Fotograf:Rob Zugaro Forskere fra RMIT University har udviklet en miljøvenlig nul-cementbeton, hvilket næsten eliminerer -
 Bekæmpelse af kræft ved nulpunktet med designermolekylerEn grafisk repræsentation af det nye molekyle (gule pinde), der interagerer med den glidende klemme (grøn overflade). Kredit:University of Adelaide Et nyt molekyle designet af forskere fra Univers
Bekæmpelse af kræft ved nulpunktet med designermolekylerEn grafisk repræsentation af det nye molekyle (gule pinde), der interagerer med den glidende klemme (grøn overflade). Kredit:University of Adelaide Et nyt molekyle designet af forskere fra Univers
- Hvad er meningen med i hvert liv, som lidt regn skal falde?
- Fysiker hædret for at finde ny symmetri i rum og tid
- Hvad betyder han i videnskabsperioden?
- Undersøgelse sporer, hvordan emissioner af træstammer fra vådområder varierer efter sæson, beli…
- Undersøgelse viser, at plastikaffald kan omdannes til energi og brændstof
- Fleksibel ultralydsplaster kan gøre det lettere at inspicere skader i ulige formede strukturer


