Hvorfor tilsat calciumchlorid i natrium for at sænke smeltepunktet?
Her er hvorfor:
* frysningspunktdepression: Tilsætningen af et opløst stof, som calciumchlorid, til et opløsningsmiddel, som natrium, sænker opløsningsmidlets frysepunkt. Dette er en kolligativ egenskab, hvilket betyder, at det kun afhænger af koncentrationen af det opløste stof, ikke dens identitet.
* Hvorfor er dette vigtigt? Det er gavnligt for forskellige anvendelser at sænke natriumens frysepunkt for forskellige anvendelser, især i produktionen af natriummetal.
* Processen:
* Natrium produceres normalt ved elektrolyse af smeltet natriumchlorid.
* Tilsætning af calciumchlorid sænker frysningspunktet for natriumchloridblandingen, hvilket gør det muligt for elektrolysen at forekomme ved en lavere temperatur.
* Dette gør processen mere energieffektiv og omkostningseffektiv.
Nøglepunkter:
* smeltepunkt: Temperaturen, hvormed en solid overgår til en væske.
* frysningspunkt: Temperaturen, hvormed en flydende overgår til et fast stof.
* frysningspunktdepression: Fænomenet, hvor frysningspunktet for et opløsningsmiddel sænkes ved tilsætning af et opløst stof.
I resumé tilsættes calciumchlorid til natrium (specifikt natriumchlorid) for at sænke sit frysepunkt, hvilket gør elektrolyseprocessen mere effektiv.
 Varme artikler
Varme artikler
-
 At give ilt til spørgsmålet om luftkvalitetFlygtige alkaner, tidligere antaget at have en mindre modtagelighed for autooxidation, er nu afsløret at have et meget mere komplekst forhold til ilt, hvilket kan have betydelige konsekvenser for bræn
At give ilt til spørgsmålet om luftkvalitetFlygtige alkaner, tidligere antaget at have en mindre modtagelighed for autooxidation, er nu afsløret at have et meget mere komplekst forhold til ilt, hvilket kan have betydelige konsekvenser for bræn -
 Forskere har fundet en måde at skabe lægemiddelmolekyler ud fra kulilteResultaterne af atomeffektivitetsreaktioner. Kredit:Denis Chusov Forskere fra RUDN Universitet har i samarbejde med russiske og udenlandske kolleger studeret reduktive amineringsreaktioner. De nye
Forskere har fundet en måde at skabe lægemiddelmolekyler ud fra kulilteResultaterne af atomeffektivitetsreaktioner. Kredit:Denis Chusov Forskere fra RUDN Universitet har i samarbejde med russiske og udenlandske kolleger studeret reduktive amineringsreaktioner. De nye -
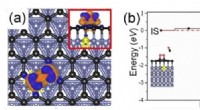 Højtydende grafenbaserede katalysatorerFigur viser (a) ladningsoverførsel mellem det understøttede grafen og det adsorberede O2 -molekyle, når substratet er dopet med en urenhed (i dette eksempel, et metalelement, farvekodet i gult). Blå (
Højtydende grafenbaserede katalysatorerFigur viser (a) ladningsoverførsel mellem det understøttede grafen og det adsorberede O2 -molekyle, når substratet er dopet med en urenhed (i dette eksempel, et metalelement, farvekodet i gult). Blå ( -
 Den molekylære afbøjning af lysstråling ved hjælp af diamantanKredit:Pixabay/CC0 Public Domain Et internationalt hold ledet af kemikeren Heinz Langhals fra Ludwig-Maximilians Universitaet (LMU) i München er lykkedes med den molekylære afbøjning af lysstrålin
Den molekylære afbøjning af lysstråling ved hjælp af diamantanKredit:Pixabay/CC0 Public Domain Et internationalt hold ledet af kemikeren Heinz Langhals fra Ludwig-Maximilians Universitaet (LMU) i München er lykkedes med den molekylære afbøjning af lysstrålin
- Forskere forbedrer vandspaltningsreaktionen til produktion af grøn brint
- Bilomkostninger gør Singapore til verdens dyreste by. Igen.
- Forudsigelsesværktøj viser, hvordan skovudtynding kan øge Sierra Nevada-snepakningen
- Hvordan er solen som alle andre stjerner?
- Erfaringer fra hollandsk geologisk historie kan være nyttige for andre nutidige deltaer
- Hvordan man fortæller fjollede guld fra Real Gold


