Hvad er ammoniumion til stede i?
uorganiske forbindelser:
* ammoniumsalte: Dette er ioniske forbindelser dannet af kombinationen af ammoniumioner med forskellige anioner, såsom chlorid (NH₄CL), sulfat ((NH₄) ₂SO₄), nitrat (NH₄no₃) og carbonat ((NH₄) ₂CO₃).
* ammoniumhydroxid (NH₄OH): Selvom det ikke er en ægte forbindelse, er det en opløsning af ammoniak (NH₃) i vand, hvor ammoniak reagerer med vand til dannelse af ammonium- og hydroxidioner.
organiske forbindelser:
* ammoniumholdige organiske forbindelser: Dette er organiske molekyler, der indeholder ammoniumioner som en del af deres struktur, såsom kvartære ammoniumsalte.
Biologiske systemer:
* nitrogencyklus: Ammoniumioner er et vigtigt mellemprodukt i nitrogencyklussen, der spiller en nøglerolle i omdannelsen af atmosfærisk nitrogen til brugbare former af mikroorganismer.
* Biomolekyler: Ammoniumioner findes også i visse biomolekyler, såsom aminosyrer (f.eks. Glutamin), som er byggestenene for proteiner.
Industrielle applikationer:
* Gødning: Ammoniumsalte bruges ofte som gødning til at tilvejebringe nitrogen til planter.
* eksplosiver: Ammoniumnitrat (NH₄no₃) er en vigtig komponent i nogle eksplosiver.
* Andre applikationer: Ammoniumioner bruges også i en række andre industrielle anvendelser, såsom produktion af plast, farvestoffer og farmaceutiske stoffer.
naturligt forekommende:
* Vulkanske gasser: Ammoniumioner findes i vulkanske gasser, hvor de produceres ud fra sammenbruddet af organisk stof.
* grundvand og overfladevand: Ammoniumioner findes i grundvand og overfladevand på grund af nedbrydningen af organisk stof og landbrugsafstrømning.
Sammenfattende er ammoniumioner allestedsnærværende i både naturlige og menneskeskabte miljøer og spiller vigtige roller i forskellige kemiske, biologiske og industrielle processer.
 Varme artikler
Varme artikler
-
 Forskere opnår nye resultater i undersøgelsen af uorganiske pigmenter med apatitstrukturPrøve af høj renhed af bariumhypomanganatchlorid. Kredit:Lobachevsky University Forbindelser med apatitstrukturen adskiller sig fra de fleste klasser ved de forskellige kemiske sammensætninger. Fo
Forskere opnår nye resultater i undersøgelsen af uorganiske pigmenter med apatitstrukturPrøve af høj renhed af bariumhypomanganatchlorid. Kredit:Lobachevsky University Forbindelser med apatitstrukturen adskiller sig fra de fleste klasser ved de forskellige kemiske sammensætninger. Fo -
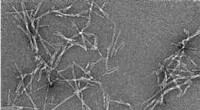 Forstå væksten af sygdomsfremkaldende proteinfibreTransmissionselektronmikrofotografi af fibriller fra proteinet alfa-synuclein, som er forbundet med Parkinsons sygdom. Kredit:University of Bath Amyloidfibriller er aflejringer af proteiner i krop
Forstå væksten af sygdomsfremkaldende proteinfibreTransmissionselektronmikrofotografi af fibriller fra proteinet alfa-synuclein, som er forbundet med Parkinsons sygdom. Kredit:University of Bath Amyloidfibriller er aflejringer af proteiner i krop -
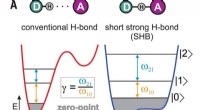 Eksperimenter med bifluoridioner viser tegn på hybridbindingerHydrogenbindinger. (A) Typer af hydrogenbindinger afhængigt af donor-acceptor afstand. Potentialer for protonbevægelse vises sammen med de tre første kvantenniveauer og de tilhørende laveste energiove
Eksperimenter med bifluoridioner viser tegn på hybridbindingerHydrogenbindinger. (A) Typer af hydrogenbindinger afhængigt af donor-acceptor afstand. Potentialer for protonbevægelse vises sammen med de tre første kvantenniveauer og de tilhørende laveste energiove -
 Ny indsigt i større sygdomsforløbKredit:CC0 Public Domain Flinders forskere har gjort store indgreb i at finde årsagen til hjertesygdomme, Alzheimers, Kræft, diabetes og andre sygdomme efter at have opdaget yderligere 148 protein
Ny indsigt i større sygdomsforløbKredit:CC0 Public Domain Flinders forskere har gjort store indgreb i at finde årsagen til hjertesygdomme, Alzheimers, Kræft, diabetes og andre sygdomme efter at have opdaget yderligere 148 protein
- Hvornår begyndte tiden ifølge teorien?
- Nye abortlove står over for COVID-19 og ressourcemæssige hindringer
- Molekyle fra naturen giver fuldt genanvendelige polymerer
- Afsløring af den mikroskopiske mekanisme af superledende metalliske transistorer
- Er mængden af forstyrrelse eller ubrugelig energi i et system?
- Opdagelsen kaster lys over det store mysterium om, hvorfor universet har mindre antistof end stof


