En jernchloridforbindelse indeholder 55,85 gram og 106,5 chlor, hvad er den mest sandsynlige empiriske formel for denne forbindelse?
1. Konverter masser til mol:
* jern (Fe): 55,85 g Fe / 55,845 g / mol Fe =1.000 mol Fe
* klor (Cl): 106,5 g Cl / 35,45 g / mol Cl =3.000 mol Cl
2. Find molforholdet:
* Opdel antallet af mol af hvert element med det mindste antal mol:
* Fe:1.000 mol / 1.000 mol =1
* Cl:3.000 mol / 1.000 mol =3
3. Skriv den empiriske formel:
* Molforholdet indikerer, at der er 1 jernatom for hvert 3. kloratomer.
* Den empiriske formel er fecl₃
 Varme artikler
Varme artikler
-
 Smeltning af skrottede enheder, da bæredygtige behov opvarmesKredit:University of Queensland Smeltning af metaller fra kasserede elektroniske enheder er blandt løsninger til bæredygtig forsyning af kritiske materialer, der undersøges af forskere fra Univers
Smeltning af skrottede enheder, da bæredygtige behov opvarmesKredit:University of Queensland Smeltning af metaller fra kasserede elektroniske enheder er blandt løsninger til bæredygtig forsyning af kritiske materialer, der undersøges af forskere fra Univers -
 Forskere udvikler en ny metode til at overvåge molekylær aggregeringSimulerede kirotiske egenskaber kontra dihedral vinkel θ af (R)1, 1-binaphthyl. Kredit:Hong Kong University of Science and Technology Chirale molekyler er defineret som molekyler, der ikke kan ove
Forskere udvikler en ny metode til at overvåge molekylær aggregeringSimulerede kirotiske egenskaber kontra dihedral vinkel θ af (R)1, 1-binaphthyl. Kredit:Hong Kong University of Science and Technology Chirale molekyler er defineret som molekyler, der ikke kan ove -
 Ny teknik til at karakterisere kemisk sammensætning og struktur af prøverKredit:Forance, Shutterstock Raman -spektroskopi er en væsentlig teknik, der bruges til undersøgelse af materialer - herunder nanostrukturer - og biologiske systemer til at analysere deres sammens
Ny teknik til at karakterisere kemisk sammensætning og struktur af prøverKredit:Forance, Shutterstock Raman -spektroskopi er en væsentlig teknik, der bruges til undersøgelse af materialer - herunder nanostrukturer - og biologiske systemer til at analysere deres sammens -
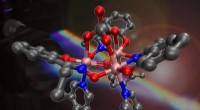 Skydatahastigheder indstillet til at svæve ved hjælp af laser-minimagneterModel af en enkelt-molekyle magnet Kredit:Dr. Olof Johansson Lille bitte, laseraktiverede magneter kan gøre det muligt for cloud computing-systemer at behandle data op til 100 gange hurtigere end
Skydatahastigheder indstillet til at svæve ved hjælp af laser-minimagneterModel af en enkelt-molekyle magnet Kredit:Dr. Olof Johansson Lille bitte, laseraktiverede magneter kan gøre det muligt for cloud computing-systemer at behandle data op til 100 gange hurtigere end


