Hvordan redegør du for disse kendsgerninger n-butylalkohol har et meget højere kogepunkt end dets isomer-di-ethylether, men begge forbindelser har den samme opløselighed i vand?
Kogepunkt:
* Hydrogenbinding: Butanol (CH3CH2CH2CH2OH) har en hydroxylgruppe (-OH), som giver den mulighed for at danne stærke brintbindinger med andre butanolmolekyler. Disse obligationer er relativt stærke og kræver en masse energi for at bryde, hvilket fører til et højere kogepunkt.
* diethylether: Diethylether (CH3CH2OCH2CH3) mangler en hydroxylgruppe. Det kan kun deltage i svagere dipol-dipol-interaktioner og London-spredningskræfter, som er meget lettere at overvinde. Dette resulterer i et markant lavere kogepunkt for diethylether.
opløselighed i vand:
* Hydrogenbinding: Mens begge forbindelser kan danne hydrogenbindinger med vandmolekyler, ligger forskellen i omfanget af brintbinding. Butanols enkelt hydroxylgruppe muliggør stærk hydrogenbinding med vand, hvilket fører til relativt god opløselighed.
* hydrofob del: Diethylether har en større hydrofob (vandafvisende) del sammenlignet med butanol. Denne hydrofobe del begrænser dens evne til at interagere med vandmolekyler effektivt, selvom den kan danne nogle brintbindinger.
* balance: Balancen mellem evnen til at danne hydrogenbindinger og størrelsen på den hydrofobe del dikterer den samlede opløselighed. I dette tilfælde er hydrogenbindingen i butanol stærk nok til at overvinde den større hydrofobe del, hvilket resulterer i lignende opløselighed som diethylether.
Kortfattet:
* kogepunkt: Butanols stærke hydrogenbinding fører til et signifikant højere kogepunkt sammenlignet med diethylether.
* opløselighed i vand: Begge forbindelser kan danne hydrogenbindinger med vand, men balancen mellem hydrogenbinding og hydrofobe interaktioner bestemmer deres samlede opløselighed. I dette tilfælde er hydrogenbindingen i butanol tilstrækkelig til at gøre det nogenlunde så opløseligt som diethylether.
Fortæl mig, hvis du har andre spørgsmål om egenskaberne ved disse forbindelser!
 Varme artikler
Varme artikler
-
 Interaktion mellem iodonium og sølvkation demonstreret for første gangSådan sker det:Positivt jod giver en elektrongave til positivt sølv. Kredit:Antonio Frontera og Kari Rissanen Et internationalt forskerhold ledet af professor Kari Rissanen fra University of Jyvas
Interaktion mellem iodonium og sølvkation demonstreret for første gangSådan sker det:Positivt jod giver en elektrongave til positivt sølv. Kredit:Antonio Frontera og Kari Rissanen Et internationalt forskerhold ledet af professor Kari Rissanen fra University of Jyvas -
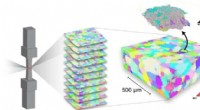 3D-eksperimenter kaster nyt lys over formhukommelseslegeringerUdviklingen af den interne mikrostruktur af en nikkel-titaniumprøve måles, mens den testes mekanisk. Farverne svarer til krystallografisk orientering, og orienteringerne er samlet i korn, eller krys
3D-eksperimenter kaster nyt lys over formhukommelseslegeringerUdviklingen af den interne mikrostruktur af en nikkel-titaniumprøve måles, mens den testes mekanisk. Farverne svarer til krystallografisk orientering, og orienteringerne er samlet i korn, eller krys -
 At manipulere med cellulære fedtstoffer lover megetSabotage med cellulære lipidmembraner giver et stort løfte. Kredit:DTU I dag, meget af den biologi, der ligger til grund for den cellulære sammensætning af lipider, er en sort boks for videnskabsm
At manipulere med cellulære fedtstoffer lover megetSabotage med cellulære lipidmembraner giver et stort løfte. Kredit:DTU I dag, meget af den biologi, der ligger til grund for den cellulære sammensætning af lipider, er en sort boks for videnskabsm -
 Discovery booster teorien om, at liv på Jorden opstod fra RNA-DNA-blandingKredit:CC0 Public Domain Kemikere ved Scripps Research har gjort en opdagelse, der understøtter et overraskende nyt syn på, hvordan liv opstod på vores planet. I en undersøgelse offentliggjort i
Discovery booster teorien om, at liv på Jorden opstod fra RNA-DNA-blandingKredit:CC0 Public Domain Kemikere ved Scripps Research har gjort en opdagelse, der understøtter et overraskende nyt syn på, hvordan liv opstod på vores planet. I en undersøgelse offentliggjort i
- Hvad beskriver bedst den måde, hvor gener kromosomer og DNA er relateret?
- Kemikalier, der bruges i retsmedicinsk videnskab
- Hvad er en del af det udskillelsessystem Annelids?
- Volvo tilbagekalder biler til at reparere automatisk bremsefejl
- Polarvandring på dværgplaneten Ceres afsløret
- Hvad er forskellen mellem transkription og DNA -replikation?


