Er bly II -sulfat ioniseret eller dissocieret i en vandig opløsning?
Her er hvorfor:
* opløselighed: Bly (ii) sulfat er en meget dårligt opløselig Forbindelse i vand. Dette betyder, at kun en lille brøkdel af den faste PBSO₄ opløses i vand.
* ionisk karakter: Mens PBSO₄ er en ionisk forbindelse, har den en meget stærk ionisk binding mellem bly (II) kation (Pb²⁺) og sulfatanionen (SO₄²⁻). Denne stærke binding gør det vanskeligt for ionerne at adskille sig i vand.
Kortfattet:
* Det meste af PBSO₄ forbliver som et solidt bundfald.
* En lille mængde pb²⁺ og so₄²⁻ ioner er til stede i opløsning, men koncentrationen er ekstremt lav.
Derfor betragtes PBSO₄ som uopløselig og ioniserer eller dissocierer ikke signifikant i vand.
Sidste artikelHvordan produceres metal fra malm?
Næste artikelHvad er produkterne fra iltgas med fossil brændstof?
 Varme artikler
Varme artikler
-
 Syntese af opiumalkaloider ved hjælp af elektrisk strømDe Mainz-baserede kemikere undersøgte det oxidative nøgletrin i biosyntesen af thebain, kodein, og morfin ved hjælp af en simpel og selvfremstillet elektrokemisk celle. Kredit:Alexander Lipp For
Syntese af opiumalkaloider ved hjælp af elektrisk strømDe Mainz-baserede kemikere undersøgte det oxidative nøgletrin i biosyntesen af thebain, kodein, og morfin ved hjælp af en simpel og selvfremstillet elektrokemisk celle. Kredit:Alexander Lipp For -
 Heliumioner åbner en helt ny verden af materialerKredit:Queensland University of Technology QUT-forskere har fundet en spændende ny måde at manipulere og designe fremtidens materialer på atomniveau og ændre den måde, de opfører sig på i større s
Heliumioner åbner en helt ny verden af materialerKredit:Queensland University of Technology QUT-forskere har fundet en spændende ny måde at manipulere og designe fremtidens materialer på atomniveau og ændre den måde, de opfører sig på i større s -
 Fluorescerende molekyle forråder nedbrydningen af polymermaterialerH-DAAN kunne fungere som en radikal scavenger for polymere mekanoradikaler i bulk og generere DAAN•, som potentielt kunne evalueres ved EPR-spektroskopi og fluorescensmålinger på grund af deres høje s
Fluorescerende molekyle forråder nedbrydningen af polymermaterialerH-DAAN kunne fungere som en radikal scavenger for polymere mekanoradikaler i bulk og generere DAAN•, som potentielt kunne evalueres ved EPR-spektroskopi og fluorescensmålinger på grund af deres høje s -
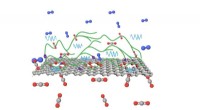 Næste generations membraner til kulstoffangstCO2-selektive polymere kæder forankret på grafen trækker effektivt CO2 fra en røggasblanding. Kredit:KV Agrawal (EPFL) CO 2 fremstillet ved afbrænding af fossile brændstoffer frigives stadig for
Næste generations membraner til kulstoffangstCO2-selektive polymere kæder forankret på grafen trækker effektivt CO2 fra en røggasblanding. Kredit:KV Agrawal (EPFL) CO 2 fremstillet ved afbrænding af fossile brændstoffer frigives stadig for
- Forskere afslører, hvordan fosfat undslipper fra aktinfilamenter
- Hvorfor siges en Firefly at være naturlig lysskilde?
- På dit mærke, sæt dig - Neutroner driver enzymreaktivitet for bedre produktion af biobrændstof
- Hvilket kemikalie bruges undertiden til at skabe cellulær plast?
- En fysiker, der bestemte klare af et elektron ved hjælp af hans olie-drop-eksperiment?
- Magnetisk tuning på nanoskala


