Hvorfor accepterer et negativt kloratom let en anden elektron?
* Elektronkonfiguration: Klor har 7 elektroner i sin yderste skal. Ved at få en elektron opnår det en stabil oktetkonfiguration og opfylder Octet -reglen. Dette gør CL- til en negativt ladet ion.
* frastødning: Tilføjelse af en anden elektron til CL- ville skabe en meget ustabil art med to ekstra elektroner i dens yderste skal. Dette ville resultere i betydelig frastødelse mellem de negativt ladede elektroner, hvilket gør det meget ugunstigt.
* Elektrostatiske kræfter: Den negative ladning på CL- afviser allerede andre negativt ladede partikler. Tiltrækning af en anden elektron ville yderligere intensivere denne frastødelse.
Kortfattet: CL- er allerede stabil med en fuld oktet og en negativ ladning. Det ville kræve en betydelig mængde energi for at overvinde den elektrostatiske frastødelse og tvinge den til at acceptere en anden elektron.
Sidste artikelHvad er antallet af protoner og elektroner i jernholdig ion?
Næste artikelEr NF4 en mulig forbindelse af nitrogen og fluor?
 Varme artikler
Varme artikler
-
 Innovativ kombination af hårde og bløde materialer forbedrer vedhæftningen til ru overfladerVedhæftning til ru overflader forbedres væsentligt ved kombinationen af to materialer. Den store model viser det grundlæggende princip og strukturen af de nye klæbemidler, hvor bløde materialer (g
Innovativ kombination af hårde og bløde materialer forbedrer vedhæftningen til ru overfladerVedhæftning til ru overflader forbedres væsentligt ved kombinationen af to materialer. Den store model viser det grundlæggende princip og strukturen af de nye klæbemidler, hvor bløde materialer (g -
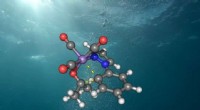 Det nye grønne alternativ til medicinproduktionStruktur af den aktive mangankatalysator i vand. Kredit:Universitetet i Göttingen De fleste af processerne til fremstilling af lægemidler, pesticider og smartphone-skærme er omkostningstunge og ge
Det nye grønne alternativ til medicinproduktionStruktur af den aktive mangankatalysator i vand. Kredit:Universitetet i Göttingen De fleste af processerne til fremstilling af lægemidler, pesticider og smartphone-skærme er omkostningstunge og ge -
 Forskere udvikler fleksibel krystal, baner vejen for mere effektiv bøjelig elektronikEt nærbillede af den nye piezoelektriske krystal udviklet af NTU -forskere, som kan bøje op til 40 gange mere end de konventionelle ferroelektriske krystaller, der typisk bruges i små aktuatorer og se
Forskere udvikler fleksibel krystal, baner vejen for mere effektiv bøjelig elektronikEt nærbillede af den nye piezoelektriske krystal udviklet af NTU -forskere, som kan bøje op til 40 gange mere end de konventionelle ferroelektriske krystaller, der typisk bruges i små aktuatorer og se -
 Ny katalysator fører til mere effektiv butadienproduktionKredit:CC0 Public Domain Forskere ved North Carolina State University har udviklet en ny katalysator, der forbedrer effektiviteten af at omdanne butan, en komponent af naturgas, til butadien - en
Ny katalysator fører til mere effektiv butadienproduktionKredit:CC0 Public Domain Forskere ved North Carolina State University har udviklet en ny katalysator, der forbedrer effektiviteten af at omdanne butan, en komponent af naturgas, til butadien - en
- Hvad vil kendskab til nettokraften på et objekt fortælle om kraftobjekt?
- Sporing af sygdomsspredning på sociale medier
- Hvordan en hård busk kunne hjælpe med at bekæmpe sult i Afrika
- Hvor lang tid tager det for sort skimmel at dræbe dig?
- Undersøgelse:Fysikere skaber kæmpe trilobit Rydberg-molekyler
- Hvem var Rube Goldberg,


