Påvirker temperaturen mængden af salt, der opløses i vand?
Her er hvorfor:
* opløselighed: Opløselighed henviser til den maksimale mængde af et stof (som salt), der kan opløses i en given mængde opløsningsmiddel (som vand) ved en bestemt temperatur.
* øget temperatur =øget opløselighed: Når temperaturen på vandet øges, bevæger molekylerne sig hurtigere og har mere energi. Denne øgede bevægelse giver dem mulighed for at bryde de ioniske bindinger fra hinanden, der holder saltkrystallerne sammen, hvilket gør det muligt for mere salt at opløses.
* Direkte forhold: Forholdet mellem temperatur og opløselighed for de fleste faste stoffer, inklusive salt, er et direkte forhold. Dette betyder, at når temperaturen går op, går opløseligheden op.
Vigtig note: Mens varmere vand opløser mere salt, er der en grænse for, hvor meget salt der kan opløses. Selv ved meget høje temperaturer er der et punkt, hvor vandet bliver mættet og ikke kan opløse mere salt.
Sidste artikelHar mursten en bestemt kemisk sammensætning?
Næste artikelHvad er antallet af protoner og elektroner i jernholdig ion?
 Varme artikler
Varme artikler
-
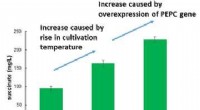 Verdens mest effektive produktion af succinat fra kuldioxidFigur 1:Øgede mængder succinat produceres baseret på overekspression af PEPC -gener og forhøjelse af dyrkningstemperaturen. Kredit:Kobe University Succinat bruges i vid udstrækning som en rå ingre
Verdens mest effektive produktion af succinat fra kuldioxidFigur 1:Øgede mængder succinat produceres baseret på overekspression af PEPC -gener og forhøjelse af dyrkningstemperaturen. Kredit:Kobe University Succinat bruges i vid udstrækning som en rå ingre -
 Forskere udvikler en katalysator til at lette selektiv omdannelse af reaktive lithiumforbindelserBochums forskningsteam har udviklet en ny katalysator, der kunne være interessant til industrielle anvendelser. Kredit:RUB, Marquard Forskere ved Ruhr-Universität Bochum har udviklet en ny katalys
Forskere udvikler en katalysator til at lette selektiv omdannelse af reaktive lithiumforbindelserBochums forskningsteam har udviklet en ny katalysator, der kunne være interessant til industrielle anvendelser. Kredit:RUB, Marquard Forskere ved Ruhr-Universität Bochum har udviklet en ny katalys -
 Prisbillig blysensor til hjemmet, byens vandledningerWen-Chi Lin viser sit elektroniske ledningssensordesign frem. Det kunne gøre det muligt for byer og husejere at lokalisere rør, der forurener vand med bly. Kredit:Evan Dougherty, Michigan Engineering
Prisbillig blysensor til hjemmet, byens vandledningerWen-Chi Lin viser sit elektroniske ledningssensordesign frem. Det kunne gøre det muligt for byer og husejere at lokalisere rør, der forurener vand med bly. Kredit:Evan Dougherty, Michigan Engineering -
 Undersøgelsen afslører detaljer om, hvordan en udbredt katalysator spalter vandIltudviklingsreaktioner er vigtige i en række industrielle processer. En ny undersøgelse giver en detaljeret analyse af processen på molekylært niveau. Som illustreret her, forskerne analyserede, hvor
Undersøgelsen afslører detaljer om, hvordan en udbredt katalysator spalter vandIltudviklingsreaktioner er vigtige i en række industrielle processer. En ny undersøgelse giver en detaljeret analyse af processen på molekylært niveau. Som illustreret her, forskerne analyserede, hvor
- Hvorfor bliver planter lysegrønne
- Nyt briefingpapir om arktisk forandring
- Sammenlign de af organismer, der respirerer til disse fotosyntisstater?
- Hvad er gitterkoordinaterne for Little Rock Arkansas?
- Indiske astronomer opdager over 200 variable stjerner
- Forskere udvikler en ny og effektiv fremstillingsteknologi til krydsformet memristor


