Hvilken gas har en densitet på 2,104 GL ved 303 K og 133 kPa ud af disse han ne ar kr xe?
1. Forstå forholdet mellem densitet, tryk og temperatur
Den ideelle gaslov hjælper os med at forstå forholdet:
* pv =nrt
Hvor:
* p =pres (i PA)
* v =volumen (i m³)
* n =antal mol
* r =ideel gas konstant (8.314 j/mol · k)
* t =temperatur (i k)
Vi kan omarrangere denne ligning for at løse for densitet (ρ):
* ρ =(n * m) / v
* ρ =(p * m) / (r * t)
Hvor:
* m =molær masse af gassen (i g/mol)
2. Konverter enheder
* tryk (p): 133 kPa =133.000 PA
* temperatur (t): 303 K (allerede i Kelvin)
3. Beregn den molære masse af hver gas
* han: 4,00 g/mol
* ne: 20,18 g/mol
* AR: 39,95 g/mol
* kr: 83,80 g/mol
* xe: 131,29 g/mol
4. Brug densitetsligningen til at finde den matchende gas
Tilslut de kendte værdier (tryk, temperatur, R) og den molære masse (M) for hver gas i densitetsligningen. Beregn densiteten for hver gas og se, hvilken der matcher den givne densitet (2,104 g/l).
Eksempel beregning (for argon):
* ρ =(p * m) / (r * t)
* ρ =(133.000 PA * 39,95 g/mol)/(8.314 J/mol · K * 303 K)
* ρ ≈ 2,104 g/l
Resultat:
Gassen med en densitet på 2,104 g/l ved 303 K og 133 kPa er argon (AR) .
Sidste artikelKan du lave brintgas selv?
Næste artikelHvor mange ioner fremstilles, når natriumsulfat opløses i vand?
 Varme artikler
Varme artikler
-
 Bladinspireret overflade forhindrer frostdannelseFrost dannes på de konvekse områder af blade, men ikke på de konkave årer. Kredit:Stephan Herb Forskere fra Northwestern University opdagede en ny måde at reducere frostdannelsen på enhver overfla
Bladinspireret overflade forhindrer frostdannelseFrost dannes på de konvekse områder af blade, men ikke på de konkave årer. Kredit:Stephan Herb Forskere fra Northwestern University opdagede en ny måde at reducere frostdannelsen på enhver overfla -
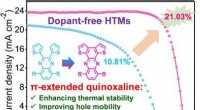 Dopantfri, fugtighedsstabile organiske lag giver perovskit solceller 21% effektivitetKredit:Wiley Holdbar, højtydende perovskit-solceller kræver også holdbare, højtydende ladningstransporterende lag. Forskere har udviklet den første organiske hultransporter, der ikke behøver et do
Dopantfri, fugtighedsstabile organiske lag giver perovskit solceller 21% effektivitetKredit:Wiley Holdbar, højtydende perovskit-solceller kræver også holdbare, højtydende ladningstransporterende lag. Forskere har udviklet den første organiske hultransporter, der ikke behøver et do -
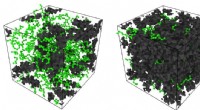 Tæt mellemrum spids tilstedeværelse af petrokemikalierSimuleringssnapshots af Rice University-ingeniører viser n-heptan-molekyler (grøn) under forskellige grader af indeslutning i en polymermatrix af molekyler (sort), hvor den højviskose polymer er en mo
Tæt mellemrum spids tilstedeværelse af petrokemikalierSimuleringssnapshots af Rice University-ingeniører viser n-heptan-molekyler (grøn) under forskellige grader af indeslutning i en polymermatrix af molekyler (sort), hvor den højviskose polymer er en mo -
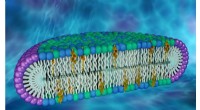 Ny cellemembranmodel kan være nøglen til at afdække nye proteinegenskaberForskere brugte neutron- og røntgenspredningsteknikker ved Oak Ridge og Brookhaven National Laboratories til at karakterisere skiveformede strukturer, kendt som biceller, der efterligner cellemembrane
Ny cellemembranmodel kan være nøglen til at afdække nye proteinegenskaberForskere brugte neutron- og røntgenspredningsteknikker ved Oak Ridge og Brookhaven National Laboratories til at karakterisere skiveformede strukturer, kendt som biceller, der efterligner cellemembrane
- Kinas rumtest rammer problemer med kapselanomali
- Forskning udforsker energi- og arealanvendelsespraksis på amerikanske golfbaner
- Fiberoptik åbner en ny grænse for jordskredsovervågning
- Vil du få teenagere til at interessere sig for matematik og naturvidenskab? Målrette deres foræld…
- At vurdere risikoen for kemikalier for dyrelivet er en kæmpe udfordring, der kræver en ny tilgang
- Hvad er anvendelsen af vandkraft energi i dag?


