Hvordan kan du finde massen af calciumcarbonat i et Tums Tablet Chemistry Lab?
Materialer:
* Tums tablet
* Bægerglas
* Gradueret cylinder
* Omrøring af stang
* Destilleret vand
* Hydrochlorsyre (HCL) opløsning (ca. 1 m)
* Burette
* Phenolphthalein -indikator
* Elektronisk balance
Procedure:
1. forberedelse:
* Vej nøjagtigt Tums -tabletten ved hjælp af den elektroniske balance. Registrer massen.
* Fyld buretten med den standardiserede HCL -løsning. Registrer det oprindelige volumen af HCL i buretten.
2. reaktion:
* Opløs Tums -tabletten i et bægerglas, der indeholder en lille mængde destilleret vand. Dette vil hjælpe med at opløse calciumcarbonatet.
* Tilføj et par dråber phenolphthalein -indikator til opløsningen. Løsningen skal blive lyserød på grund af tilstedeværelsen af basen i Tums -tabletten.
* Tilføj langsomt HCL fra buretten til Tums -opløsningen, mens du konstant omrøres.
* Fortsæt med at tilføje HCL, indtil den lyserøde farve forsvinder helt. Dette indikerer, at calciumcarbonatet har reageret fuldstændigt med HCL.
3. titrering:
* Registrer det endelige bind af HCL i buretten. Beregn volumenet af HCL, der bruges ved at trække det oprindelige volumen fra det endelige bind.
4. Beregninger:
* mol HCL: Brug molariteten af HCL -opløsningen og det volumen, der bruges til at beregne molen af HCL, der reagerede.
* mol Caco3: Reaktionen mellem calciumcarbonat og saltsyre er:
CACO3 (S) + 2 HCI (AQ) → CACL2 (AQ) + H2O (L) + CO2 (G)
Molforholdet mellem CACO3 og HCL er 1:2. Derfor er molen af CaCO3 reageret halvdelen af molen af HCL anvendt.
* Mass af Caco3: Beregn massen af CaCO3 ved hjælp af dens molære masse (100,09 g/mol). Multiplicer molen af CaCO3 med dens molære masse for at få massen af CaCO3 i tabletten.
5. Procentdel af CACO3:
* Opdel massen af CACO3 med den originale masse af tums -tabletten og multiplicer med 100 for at beregne procentdelen af CACO3 i tabletten.
Sikkerhedsforholdsregler:
* Bær passende beskyttelsesbriller og handsker, mens du håndterer kemikalier.
* Arbejd i et godt ventileret område.
* Bortskaf kemikalier korrekt.
Yderligere noter:
* Nøjagtigheden af dette eksperiment afhænger af nøjagtigheden af den standardiserede HCL -opløsning og titreringsprocessen.
* Det kan være nødvendigt at justere mængden af destilleret vand og HCL -opløsning anvendt afhængigt af størrelsen på Tums -tabletten.
* Dette eksperiment tilvejebringer et estimering af calciumcarbonatindholdet i Tums -tabletten. Det faktiske beløb kan variere lidt.
Fortæl mig, hvis du har andre spørgsmål.
 Varme artikler
Varme artikler
-
 Selvvandende jord kan ændre landbrugetForskere plantede radiser i dette miniaturedrivhus ved hjælp af deres selvvandende jord og sammenlignede det med sandjord, der findes i tørre områder af verden. Kredit:University of Texas i Austin
Selvvandende jord kan ændre landbrugetForskere plantede radiser i dette miniaturedrivhus ved hjælp af deres selvvandende jord og sammenlignede det med sandjord, der findes i tørre områder af verden. Kredit:University of Texas i Austin -
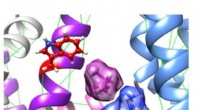 Forskere opdager molekylære mekanismer af gamle naturlægemidlerComputermodel af de to urtekomponenter, et isovalerinsyremolekyle (violet, øverst til venstre) og mallotoksin (blå, nederst til højre), optager tilstødende bindingssteder for synergistisk at aktivere
Forskere opdager molekylære mekanismer af gamle naturlægemidlerComputermodel af de to urtekomponenter, et isovalerinsyremolekyle (violet, øverst til venstre) og mallotoksin (blå, nederst til højre), optager tilstødende bindingssteder for synergistisk at aktivere -
 Springende firben:Forskning tester grænserne for gekko-adhæsionEn tokay gekko, der klamrer sig til en glat overflade. Kredit:William Stewart Mange gekkoer bor i træer, bor ofte højt i baldakinen. Stoler på deres utrolige klæbestyrke for at hjælpe dem med at b
Springende firben:Forskning tester grænserne for gekko-adhæsionEn tokay gekko, der klamrer sig til en glat overflade. Kredit:William Stewart Mange gekkoer bor i træer, bor ofte højt i baldakinen. Stoler på deres utrolige klæbestyrke for at hjælpe dem med at b -
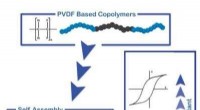 Ferroelektriske polymerer gjort mere alsidigeEn blokcopolymer af PVDF (sort) og en isolerende polymerkæde (blå) danner en blokcopolymer. Gennem faseadskillelse, blokkene samles i film. De dielektriske egenskaber kan indstilles ved at variere sam
Ferroelektriske polymerer gjort mere alsidigeEn blokcopolymer af PVDF (sort) og en isolerende polymerkæde (blå) danner en blokcopolymer. Gennem faseadskillelse, blokkene samles i film. De dielektriske egenskaber kan indstilles ved at variere sam
- Ski-værdigt eksoskelet sæt til at forbedre oplevelsen
- Nye strategier for bæredygtigt og rentabelt husdyrbrug
- Atomfysikere på jagt efter sammenpressede protoner
- Hvad er mindre end en millimeter?
- Japanske forskere udvikler ultratynde, meget elastisk huddisplay
- Hvorfor er videnskabskoncepter vigtige i din hverdag?


