Hvad er antallet af klorioner i 0,5 mol titanium 3 chlorid?
1. Forståelse af formlen:
* ticl₃ Angiver, at hver formelenhed for titanium (III) chlorid indeholder en titanion (Ti³⁺) og tre chloridioner (CL⁻).
2. Mol til ioner:
* avogadros nummer: 6,022 x 10²³ er antallet af partikler (atomer, molekyler, ioner osv.) I en mol af et stof.
* Da der er 3 cl⁻ioner pr. Ticl₃ -formelenhed, vil 0,5 mol ticl₃ indeholde:0,5 mol ticl₃ * 3 cl⁻ioner/ticl₃ =1,5 mol cl⁻ioner
3. Beregn antallet af ioner:
* Antal Cl⁻ioner: 1,5 mol cl⁻ * (6,022 x 10²³ Cl⁻ioner/mol cl⁻) =9,033 x 10²³ Cl⁻ioner
Derfor er der ca. 9,033 x 10²³ chloridioner i 0,5 mol titanium (III) chlorid.
Sidste artikelHvad er biprodukterne af syntese n-butylbromid?
Næste artikelHvad er NASO -sammensætning?
 Varme artikler
Varme artikler
-
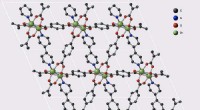 Nye materialer til opbevaring af brændbare industrigasserStruktur af metal-organisk rammeværk MOF-508, sammensat af kulstof (sort), nitrogen (blå), oxygen (rød) og zink (grøn). Fleksibiliteten og den kædede karakter af denne ramme er nøgleparametre for opbe
Nye materialer til opbevaring af brændbare industrigasserStruktur af metal-organisk rammeværk MOF-508, sammensat af kulstof (sort), nitrogen (blå), oxygen (rød) og zink (grøn). Fleksibiliteten og den kædede karakter af denne ramme er nøgleparametre for opbe -
 Ny teknik, hvor lægemidler får bakterier til at lyse, kan hjælpe med at bekæmpe antibiotikaresis…Lægemiddeloptagelse i bakterier før og efter. Kredit:Dr Stefano Pagliara, University of Exeter En ny teknik kan hjælpe med at reducere antibiotikaudskrivning ved at forudsige, hvilke lægemidler de
Ny teknik, hvor lægemidler får bakterier til at lyse, kan hjælpe med at bekæmpe antibiotikaresis…Lægemiddeloptagelse i bakterier før og efter. Kredit:Dr Stefano Pagliara, University of Exeter En ny teknik kan hjælpe med at reducere antibiotikaudskrivning ved at forudsige, hvilke lægemidler de -
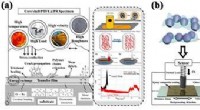 Udvikling af kerne-skal funktionelle kompositter med fremragende selvsmørende egenskaberForberedelse og friktionsoverførselsmekanisme af PTFE-baserede kerne-skal komposit smørematerialer med miljøtilpasning til flere arbejdsforhold. Kredit:LICP I takt med at avanceret mekanisk udstyr
Udvikling af kerne-skal funktionelle kompositter med fremragende selvsmørende egenskaberForberedelse og friktionsoverførselsmekanisme af PTFE-baserede kerne-skal komposit smørematerialer med miljøtilpasning til flere arbejdsforhold. Kredit:LICP I takt med at avanceret mekanisk udstyr -
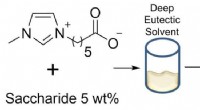 Nye opløsningsmidler til at nedbryde plantecellulose til bioethanolEgnede opløsningsmidler er nødvendige for at fremstille ethanol fra celluloseholdig plantebiomasse. Vi har fundet ud af, at flydende zwitterioner er velegnede til det, men det har været vanskeligt at
Nye opløsningsmidler til at nedbryde plantecellulose til bioethanolEgnede opløsningsmidler er nødvendige for at fremstille ethanol fra celluloseholdig plantebiomasse. Vi har fundet ud af, at flydende zwitterioner er velegnede til det, men det har været vanskeligt at
- Hvilken kropsdel konverterer mad til energi?
- Hybrider taber kant, men Edmunds vælger 5, der stadig er værd at købe
- Løver, chimpanser, hajer får ekstra beskyttelse i henhold til FN-konventionen
- Mikroskopiske enheder, der styrer vibrationer, kan tillade mindre mobile enheder
- Højere opløsning i havmodeller:Er det det værd?
- Ville folk være villige til at give deres personlige data til forskning?


