Hvilket element er mest reaktivt med svovl?
Her er hvorfor:
* Elektronegativitet: Fluor er det mest elektronegative element på den periodiske tabel. Dette betyder, at det har en stærk attraktion for elektroner. Når du reagerer med svovl, trækker fluor let elektroner væk fra svovl og danner en stærk binding.
* obligationsstyrke: S-F-bindingen er meget stærk på grund af den høje elektronegativitetsforskel mellem svovl og fluor.
* Oxidationstilstand: Fluor oxideres let svovl, hvilket betyder, at det får svovl til at miste elektroner og blive positivt ladet.
Mens andre halogener (klor, brom og jod) også reagerer med svovl, gør Fluoras højere elektronegativitet det til det mest reaktive.
Sidste artikelHvorfor er en brint kerne -ladning?
Næste artikelEr en stofblandingsforbindelse eller et element?
 Varme artikler
Varme artikler
-
 Vand hjælper med den uventede og ultrahurtige syntese af kollagenlignende syntetisk poly-L-prolinKredit:CC0 Public Domain I arbejde offentliggjort online for nylig i National Science Review, et hold ledet af prof. Hua Lu fra College of Chemistry and Molecular Engineering ved Peking University
Vand hjælper med den uventede og ultrahurtige syntese af kollagenlignende syntetisk poly-L-prolinKredit:CC0 Public Domain I arbejde offentliggjort online for nylig i National Science Review, et hold ledet af prof. Hua Lu fra College of Chemistry and Molecular Engineering ved Peking University -
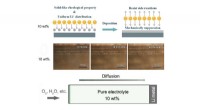 Hydrofob silica kolloid elektrolyt lover sikrere lithium-oxygen batterierSkematisk graf og eksperimentelle data, der viser den lithiumdendritforebyggende effekt af 10 vægt% HSCE. Skematisk graf og eksperimentelle data, der viser antikorrosionseffekten af 10 vægt% HSCE. K
Hydrofob silica kolloid elektrolyt lover sikrere lithium-oxygen batterierSkematisk graf og eksperimentelle data, der viser den lithiumdendritforebyggende effekt af 10 vægt% HSCE. Skematisk graf og eksperimentelle data, der viser antikorrosionseffekten af 10 vægt% HSCE. K -
 Svovlindhold i nogle højtydende stoffer svækker dem, når de udsættes for fugtPh.d.-studerende Saiful Hoque ledede ny forskning, der kunne vise vejen til at udvikle stærkere, sikrere beskyttelsestøj til brandmænd og andre arbejdere. Kredit:University of Alberta Forskere har
Svovlindhold i nogle højtydende stoffer svækker dem, når de udsættes for fugtPh.d.-studerende Saiful Hoque ledede ny forskning, der kunne vise vejen til at udvikle stærkere, sikrere beskyttelsestøj til brandmænd og andre arbejdere. Kredit:University of Alberta Forskere har -
 Skaller og grapefrugter inspirerer til først fremstillet ikke-skærbart materialeKredit:CC0 Public Domain Ingeniører har hentet deres inspiration fra skaller og grapefrugter til at skabe, hvad de siger er det første fremstillede ikke-skærbare materiale. Dette nye materiale, s
Skaller og grapefrugter inspirerer til først fremstillet ikke-skærbart materialeKredit:CC0 Public Domain Ingeniører har hentet deres inspiration fra skaller og grapefrugter til at skabe, hvad de siger er det første fremstillede ikke-skærbare materiale. Dette nye materiale, s
- Ændringer i trækronen lettede udviklingen af det første glidende krybdyr nogensinde, antyder ny…
- Recessioner gør unge mennesker arr hele livet, selv på pension
- Hvad er oxidationstallet for NHO3?
- Californiens vandmyndigheder ved ikke, hvor meget deres rør lækker, viser rapporten
- Hvilke metoder bruger forskere til at spore tornadoer?
- Lægemiddelbærere i nanostørrelse kan være fremtiden for patienter med lungesygdom


