Er ammoniumcarbonat et uopløseligt salt?
Her er hvorfor:
* ammoniumsalte er generelt opløselige. Ammonium (NH₄⁺) er en positivt ladet ion, der danner ioniske bindinger med negativt ladede anioner. Disse bindinger er normalt svage nok til at give saltet mulighed for at opløses i vand.
* carbonatsalte er typisk uopløselige med undtagelser. Mens de fleste carbonater er uopløselige, er ammoniumcarbonat en undtagelse fra denne regel. Dette skyldes den stærke tendens hos ammoniumioner til at danne opløselige forbindelser.
Derfor opløses ammoniumcarbonat let i vand, hvilket gør det til et opløseligt salt.
Sidste artikelHvad er farven på ammoniumcarbonat?
Næste artikelVil ammoniumion danne et uopløseligt salt med carbonat?
 Varme artikler
Varme artikler
-
 Hurtig 3D-print med synligt lysDette komplekse objekt blev 3D-printet på omkring 2,5 timer ved hjælp af synligt lys. Kredit:Tilpasset fra ACS Central Science 2020, DOI:10.1021/acscentsci.0c00929 3-D-print har drevet innovatio
Hurtig 3D-print med synligt lysDette komplekse objekt blev 3D-printet på omkring 2,5 timer ved hjælp af synligt lys. Kredit:Tilpasset fra ACS Central Science 2020, DOI:10.1021/acscentsci.0c00929 3-D-print har drevet innovatio -
 Ny membran adskiller spejlede molekyler effektivtIllustration af den chirale membran til selektiv permeation. Kredit:LIU Bos team Prof. Liu Bo og kolleger ved University of Science and Technology of China (USTC) har udviklet en chiral separation
Ny membran adskiller spejlede molekyler effektivtIllustration af den chirale membran til selektiv permeation. Kredit:LIU Bos team Prof. Liu Bo og kolleger ved University of Science and Technology of China (USTC) har udviklet en chiral separation -
 Forskere dyrker hurtigt en langfrøet DKDP-krystalStor langfrøet DKDP-krystal med et langt frø. Kredit:SIOM DKDP (KD x H 2-x PO 4 ), som kan minimere stimuleret Raman -spredning, er den bedste ikke -lineære krystal, der bruges som en triple
Forskere dyrker hurtigt en langfrøet DKDP-krystalStor langfrøet DKDP-krystal med et langt frø. Kredit:SIOM DKDP (KD x H 2-x PO 4 ), som kan minimere stimuleret Raman -spredning, er den bedste ikke -lineære krystal, der bruges som en triple -
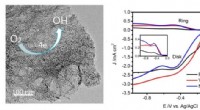 Ny elektrokatalysator udviklet til iltreduktionsreaktionVanadiumnitrid kvanteprikker forankret homogent på nitrogen-doteret grafen (VNQD-NG) blev fremstillet. De unikke strukturelle træk ved VNQD-NG inklusive de rigelige VN-kvantepunkter, højt overfladeare
Ny elektrokatalysator udviklet til iltreduktionsreaktionVanadiumnitrid kvanteprikker forankret homogent på nitrogen-doteret grafen (VNQD-NG) blev fremstillet. De unikke strukturelle træk ved VNQD-NG inklusive de rigelige VN-kvantepunkter, højt overfladeare
- Hvad er satellitternes vigtigste energikilde?
- Et firma i Dallas ønsker at bruge tankelæsende teknologi til at lade verden høre nonverbale folks…
- Det Døde Havs puls
- Hvad er planetarisk kondens?
- Hvorfor var NASA -form?
- Arkæologiske udgravninger i Rumænien viser livet for de tidligste moderne mennesker i Europa


