Hvor mange hydrogenatomer er i 6,00 mol ammoniumsulfid?
1. Kemisk formel:
* Ammoniumsulfid har den kemiske formel (NH₄) ₂s.
2. Hydrogenatomer pr. Molekyle:
* Hver ammoniumion (NH₄⁺) indeholder 4 hydrogenatomer.
* Der er to ammoniumioner i hvert molekyle af ammoniumsulfid.
* Derfor har hvert molekyle af ammoniumsulfid 4 * 2 =8 hydrogenatomer.
3. Avogadros nummer:
* Avogadros nummer fortæller os, at der er 6,022 x 10²³ molekyler i en mol af ethvert stof.
4. Beregning:
* Start med antallet af mol ammoniumsulfid:6,00 mol
* Multiplicer med Avogadros nummer for at finde antallet af molekyler:6,00 mol * (6,022 x 10²³ molekyler/mol) =3,61 x 10²⁴ Molekyler
* Multiplicer antallet af molekyler med antallet af brintatomer pr. Molekyle:3,61 x 10²⁴ Molekyler * 8 Hydrogenatomer/molekyle =2,89 x 10²⁵ Hydrogenatomer
Svar: Der er cirka 2,89 x 10²⁵ hydrogenatomer i 6,00 mol ammoniumsulfid.
Sidste artikelHvor mange atomer i ammoniumchlorid?
Næste artikelHvor mange hydrogenatomer findes i formlen for ammoniumsulfat?
 Varme artikler
Varme artikler
-
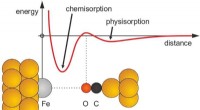 Indledende frastødning i kemisk binding udelukker ikke efterfølgende tiltrækningOvergang fra en svag fysisk binding (fysiskorption) til en stærk kemisk binding (kemisorption). Filosoffen Arthur Schopenhauer formulerede en metafor kaldet porcupine dilemma, hvilket forklarer en
Indledende frastødning i kemisk binding udelukker ikke efterfølgende tiltrækningOvergang fra en svag fysisk binding (fysiskorption) til en stærk kemisk binding (kemisorption). Filosoffen Arthur Schopenhauer formulerede en metafor kaldet porcupine dilemma, hvilket forklarer en -
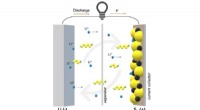 Forskere sætter opløsningen i opløsningsmiddel til lithium-svovl batteriudfordringDette diagram viser et lithium-svovlbatteri under afladning. Forskere var i stand til at observere, hvordan en bestemt type elektrolytmateriale kan reducere pendlingen af polysulfidforbindelser (vis
Forskere sætter opløsningen i opløsningsmiddel til lithium-svovl batteriudfordringDette diagram viser et lithium-svovlbatteri under afladning. Forskere var i stand til at observere, hvordan en bestemt type elektrolytmateriale kan reducere pendlingen af polysulfidforbindelser (vis -
 Låst bevægelse i molekylær motor og rotorUniversity of Groningen professor i organisk kemi Ben Feringa. Kredit:University of Groningen / Jeroen van Kooten For at en motor skal drive maskineri, den lokale bevægelse skal oversættes til den
Låst bevægelse i molekylær motor og rotorUniversity of Groningen professor i organisk kemi Ben Feringa. Kredit:University of Groningen / Jeroen van Kooten For at en motor skal drive maskineri, den lokale bevægelse skal oversættes til den -
 Studer polyfarmakologi tidligere i lægemiddelopdagelsen, siger forskereKredit:CC0 Public Domain Polyfarmakologi - et lægemiddels evne til at påvirke mere end ét protein - bør studeres tidligt i lægemiddelopdagelsesforløbet, og konstant overvåget, da den kemiske struk
Studer polyfarmakologi tidligere i lægemiddelopdagelsen, siger forskereKredit:CC0 Public Domain Polyfarmakologi - et lægemiddels evne til at påvirke mere end ét protein - bør studeres tidligt i lægemiddelopdagelsesforløbet, og konstant overvåget, da den kemiske struk
- Hvad er diagrammet, der klassificerer stjerner på en temperaturluminositetsgraf?
- Er der erosion i tundraen?
- Hvad er den samlede effekt af solen?
- Er du sikker på lyn, hvis det ikke tordner?
- Dune:Hvad klimaet i Arrakis kan fortælle os om jagt på beboelige exoplaneter
- Hvad kan nanoteknologi lære af grøn kemi


