Hvad sker der i diffusionen af vandig ammoniakkoncentreret saltsyre?
Her er en sammenbrud af, hvad der sker:
1. diffusion: Både ammoniak og saltsyre er gasser, der opløses i vand. Når de er i nærheden, diffunderer deres molekyler, der bevæger sig fra områder med høj koncentration til områder med lav koncentration.
2. reaktion: Ammoniak (NH 3 ) er en base, og saltsyre (HCI) er en syre. Når de kommer i kontakt, reagerer de i en neutraliseringsreaktion:
`` `
NH 3 (G) + HCL (aq) → NH 4 Cl (s)
`` `
3. Dannelse af ammoniumchlorid: Reaktionen producerer ammoniumchlorid (NH 4 Cl), et hvidt fast stof. Dette faste stof dannes oprindeligt som små partikler, der vises som hvide dampe Fordi de er suspenderet i luften.
4. opløsning: Over tid opløses ammoniumchloridpartiklerne i vandet og danner en opløsning.
Visualisering af reaktionen:
Du kan observere denne reaktion ved at holde en glasstang dyppet i koncentreret saltsyre nær en beholder med vandig ammoniak. De hvide dampe af ammoniumchlorid vil let være synlige, hvilket betyder, at reaktionen finder sted.
Vigtig note: Denne reaktion er eksoterm, hvilket betyder, at den frigiver varme. Det kan være farligt, hvis det ikke håndteres omhyggeligt. Arbejd altid i et godt ventileret område og undgå direkte kontakt med kemikalierne.
Sidste artikelHvorfor danner hydrogenchlorid ikke binding?
Næste artikelHvordan går elementer til fra forbindelser?
 Varme artikler
Varme artikler
-
 Team udvikler en familie af bioinspirerede kunstige træsorter fra traditionelle harpikserDet illustrerer, hvordan kunstige træsorter dannes i molekylær skala og detaljer. Kredit:YU Shuhong Naturen har givet inspirationen til design og fremstilling af højtydende biomimetiske ingeniørma
Team udvikler en familie af bioinspirerede kunstige træsorter fra traditionelle harpikserDet illustrerer, hvordan kunstige træsorter dannes i molekylær skala og detaljer. Kredit:YU Shuhong Naturen har givet inspirationen til design og fremstilling af højtydende biomimetiske ingeniørma -
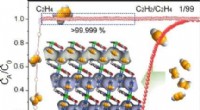 Adskillelse af sporacetylen fra ethylen i ultramikroporøse metal-organiske rammerKredit:Angewandte Chemie Ethylen, en vigtig råvare i den kemiske industri, indeholder ofte spor af acetylenforureninger, som skal fjernes. I journalen Angewandte Chemie , forskere beskriver en r
Adskillelse af sporacetylen fra ethylen i ultramikroporøse metal-organiske rammerKredit:Angewandte Chemie Ethylen, en vigtig råvare i den kemiske industri, indeholder ofte spor af acetylenforureninger, som skal fjernes. I journalen Angewandte Chemie , forskere beskriver en r -
 Bedre benzenføling ved laserpunktetSensoren udviklet af KAUST-forskere kan detektere benzen i koncentrationer, der er tre størrelsesordener lavere end konventionelle benzensensorer. Kredit:KAUST; Anastasia Serin En laserbaseret sen
Bedre benzenføling ved laserpunktetSensoren udviklet af KAUST-forskere kan detektere benzen i koncentrationer, der er tre størrelsesordener lavere end konventionelle benzensensorer. Kredit:KAUST; Anastasia Serin En laserbaseret sen -
 En ny metode til installation af svovl i komplekse molekylerForskere, der arbejder i laboratoriet i Ben Shen, Ph.d., hos Scripps Research, Florida har fundet en ny familie af svovlinstallerende enzymer ved at udvinde bakteriernes genomer i deres samling af mik
En ny metode til installation af svovl i komplekse molekylerForskere, der arbejder i laboratoriet i Ben Shen, Ph.d., hos Scripps Research, Florida har fundet en ny familie af svovlinstallerende enzymer ved at udvinde bakteriernes genomer i deres samling af mik
- Hvad beskriver bedst Jordens nordmagnet?
- Waymo slår sig sammen med Renault, Nissan på robotakse uden for USA
- Hvordan er korn i forskellige størrelser påvirket af vind erosion?
- Nøjagtig antitumorstrategi opnået via foto-switchable lanthanid-doterede nanopartikler
- Hvad er tre lag?
- Hvad er forbindelsen mellem energi fra vandpartikler ved højere temperaturer og den resulterende op…


