Er ammoniumchloridopløselig i ethanol?
Her er hvorfor:
* Polaritet: Ammoniumchlorid er en meget polær ionisk forbindelse. Ethanol er et polært opløsningsmiddel, men dets polaritet er ikke stærk nok til at overvinde de stærke ioniske kræfter, der holder ammoniumchloridet sammen.
* Hydrogenbinding: Ammoniumchlorid danner stærke brintbindinger med vand, hvilket er et mere polært opløsningsmiddel. Ethanol har i stand til hydrogenbinding, svagere brintbindingsinteraktioner end vand.
Kortfattet: Opløseligheden af ammoniumchlorid i ethanol er begrænset på grund af de stærke ioniske bindinger i forbindelsen og den svagere polaritet og hydrogenbindingskapacitet af ethanol sammenlignet med vand.
Sidste artikelWhat compound is Si3F3?
Næste artikelHvor mange gram er der i 8,2 x 1022 molekyler af NCL3?
 Varme artikler
Varme artikler
-
 Fedtsyreråvarer muliggør en højeffektiv glyoxylat-TCA-cyklus til højudbytteproduktion af β-alan…(A) Sammenligning af metaboliske veje for bioproduktion af C4 tricarboxylsyre (TCA) cyklus mellemprodukter (OAA) fra FA eller glucose råvarer. (B) Design af glyoxylat-TCA-cyklus til effektiv produktio
Fedtsyreråvarer muliggør en højeffektiv glyoxylat-TCA-cyklus til højudbytteproduktion af β-alan…(A) Sammenligning af metaboliske veje for bioproduktion af C4 tricarboxylsyre (TCA) cyklus mellemprodukter (OAA) fra FA eller glucose råvarer. (B) Design af glyoxylat-TCA-cyklus til effektiv produktio -
 Krystallisering blev krystalklarKorrelation mellem cryo-transmission elektronmikroskop (TEM) billeder og krystalstrukturen. a) TEM -billede, der viser tre kolliderende klynger. Skalaen er 10 nm. b) Relative positioner af molekyler a
Krystallisering blev krystalklarKorrelation mellem cryo-transmission elektronmikroskop (TEM) billeder og krystalstrukturen. a) TEM -billede, der viser tre kolliderende klynger. Skalaen er 10 nm. b) Relative positioner af molekyler a -
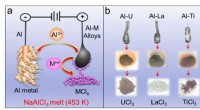 Forskere foreslår IAP-proces til adskillelse af aluminiumslegeringerFigur:IAP-proces. (a) Skematisk illustration af IAP-processen i NaAlCl4-smeltet saltelektrolyt. (b) Forskellige legeringer og tilsvarende metalchlorider udfældet i bunden af digelen ved elektrolyse
Forskere foreslår IAP-proces til adskillelse af aluminiumslegeringerFigur:IAP-proces. (a) Skematisk illustration af IAP-processen i NaAlCl4-smeltet saltelektrolyt. (b) Forskellige legeringer og tilsvarende metalchlorider udfældet i bunden af digelen ved elektrolyse -
 Dæmpning af havplastikKredit:CC0 Public Domain Efterhånden som mennesker i udviklingslandene bliver mere velhavende, de ender med at købe mere plastik. Men disse områder har ofte ikke gode affaldshåndteringsprocedurer
Dæmpning af havplastikKredit:CC0 Public Domain Efterhånden som mennesker i udviklingslandene bliver mere velhavende, de ender med at købe mere plastik. Men disse områder har ofte ikke gode affaldshåndteringsprocedurer
- Hvad mineral gør det muligt for blodet at bære ilt?
- Undersøgelse udforsker, hvordan nøglegenet modulerer terpenaroma i druer
- Hvad er en sammensat erklæring i Delphi?
- Geoteknik, andre teknologier løser ikke klimaproblemer
- En bedre forståelse af rummet - via helikopter
- Banebrydende grafenproduktion kan udløse revolution inden for udvikling af kunstig hud


