Hvad er produktet, når AGBR reagerer med NH4OH?
AGBR (S) + 2 NH4OH (AQ) ⇌ [AG (NH3) 2] + (AQ) + BR- (AQ) + 2 H2O (L)
Her er sammenbruddet:
* AGBR (er) :Sølvbromid er et lysegult fast stof, praktisk talt uopløseligt i vand.
* NH4OH (aq) :Ammoniumhydroxid er en svag base, der findes i ligevægt med ammoniak (NH3) og vand.
* [AG (NH3) 2]+ (aq) :Dette er diamminerilver (i) ion, en farveløs kompleks ion dannet af reaktionen. Det er opløseligt i vand.
* br- (aq) :Bromidioner frigøres i opløsningen.
* H2O (L) :Vand produceres som et biprodukt af reaktionen.
Det centrale punkt er, at sølvbromidet opløses i nærvær af ammoniumhydroxid på grund af dannelsen af den opløselige diamminerilver (I) kompleks ion. Denne reaktion er et eksempel på en kompleksationsreaktion .
Vigtig note: Reaktionen er en ligevægtsreaktion, hvilket betyder, at den kan fortsætte i begge retninger. Tilsætningen af overskydende ammoniumhydroxid vil favorisere dannelsen af diamminerilver (I) -komplekset, føre reaktionen fremad og opløse mere AgBR.
Sidste artikelHvad er duktiliteten af klor?
Næste artikelEr svovl en god leder af elektricitet?
 Varme artikler
Varme artikler
-
 Kemikere skaber nyt kunstigt enzymVed hjælp af beregningskemi, kandidatstuderende Vindi M. Jayasinghe-Arachchige og Rajeev Prabhakar, professor i kemi, designet et nyt molekyle, der betydeligt kunne fremme undersøgelsen og anvendelsen
Kemikere skaber nyt kunstigt enzymVed hjælp af beregningskemi, kandidatstuderende Vindi M. Jayasinghe-Arachchige og Rajeev Prabhakar, professor i kemi, designet et nyt molekyle, der betydeligt kunne fremme undersøgelsen og anvendelsen -
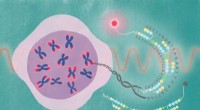 Nær-infrarød sonde afkoder telomerdynamikEn fluorescerende forbindelse blev knyttet til PIPet, der er målrettet mod den gentagne DNA -sekvens, der findes i telomerer. Denne sonde, kaldet SiR-TTet59B, muliggør observation af telomerer i aktio
Nær-infrarød sonde afkoder telomerdynamikEn fluorescerende forbindelse blev knyttet til PIPet, der er målrettet mod den gentagne DNA -sekvens, der findes i telomerer. Denne sonde, kaldet SiR-TTet59B, muliggør observation af telomerer i aktio -
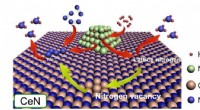 Fyldning af hulrummet i ammoniaksyntese:Nitrogenniveauernes rolle i katalysatorerNikkelpartikler dissocierer H2 for at tilvejebringe H -atomer til enten N -atomer fra selve CeN -krystalgitteret eller fremspringende N -atomer fra N2 -molekyler, der udfylder et nitrogenrum. I dette
Fyldning af hulrummet i ammoniaksyntese:Nitrogenniveauernes rolle i katalysatorerNikkelpartikler dissocierer H2 for at tilvejebringe H -atomer til enten N -atomer fra selve CeN -krystalgitteret eller fremspringende N -atomer fra N2 -molekyler, der udfylder et nitrogenrum. I dette -
 Forskere udvikler cellesugende teknologiPrikker i Histogram Feature Quantities svarer til hver celle. Vælg og klik på prikkerne på histogrammet for at bestemme, hvilke celler der skal suges. T baseret på de forudindstillede funktionsmængder
Forskere udvikler cellesugende teknologiPrikker i Histogram Feature Quantities svarer til hver celle. Vælg og klik på prikkerne på histogrammet for at bestemme, hvilke celler der skal suges. T baseret på de forudindstillede funktionsmængder
- Formuleres kemiske bindinger, når valenselektroner deles mellem atomer?
- Forskere introducerer ny metode til overvågning af Indian Summer Monsoon
- Hvor mange joules energi vil en lagerbeholdningsvarmer, der er klassificeret til 1500 watt, bruge i …
- Hvilken af disse er en gruppering af milliarder stjerner, gas og støv, der holdes sammen af tyn…
- Dybhavsminedrift forårsager massivt tab af arter, der varer i årtier
- Vi bør bruge centralt trykunderskud, ikke vindhastighed, at forudsige orkanskader


