Er svovl en god leder af elektricitet?
Her er hvorfor:
* Ikke-metallisk natur: Svovl er en ikke-metal, og ikke-metaller har generelt dårlig elektrisk ledningsevne.
* kovalent binding: Svovlatomer danner stærke kovalente bindinger inden for dens struktur, som tæt holder elektroner på plads. Dette forhindrer den frie bevægelse af elektroner, der er nødvendige for elektrisk ledningsevne.
* fravær af frie elektroner: I modsætning til metaller har svovl ikke frie elektroner i sin struktur. Dette begrænser dens evne til at transportere elektrisk ladning.
I modsætning hertil er metaller fremragende ledere af elektricitet, fordi de har et "hav" af frie elektroner, der let kan bevæge sig gennem deres struktur.
 Varme artikler
Varme artikler
-
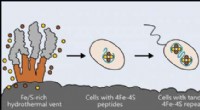 Forskere identificerer oprindelsen af metabolismeLivet kan være opstået i nærheden af hydrotermiske ventilationsåbninger rige på jern og svovl. De tidligste celler inkorporerede disse elementer i små peptider, som blev de første og enkleste ferred
Forskere identificerer oprindelsen af metabolismeLivet kan være opstået i nærheden af hydrotermiske ventilationsåbninger rige på jern og svovl. De tidligste celler inkorporerede disse elementer i små peptider, som blev de første og enkleste ferred -
 Vand, jordanalyseteknologi kan hjælpe med at forbedre oprydning og overvågning på forurenede Supe…Kredit:CC0 Public Domain Mindst 53 millioner amerikanere, inklusive omkring 18 procent af landets børn, bor mindre end tre miles fra en Superfund-side, ifølge Miljøstyrelsen. Kongressen oprettede
Vand, jordanalyseteknologi kan hjælpe med at forbedre oprydning og overvågning på forurenede Supe…Kredit:CC0 Public Domain Mindst 53 millioner amerikanere, inklusive omkring 18 procent af landets børn, bor mindre end tre miles fra en Superfund-side, ifølge Miljøstyrelsen. Kongressen oprettede -
 Gymnasieelever udvikler et billigt filter til at fjerne bly fra postevandetGymnasieelever udviklede et filter (hvis indersiden er vist her), der fastgøres til en vandhane og fjerner bly fra postevandet. Kredit:Rebecca Bushway Den næste generation af videnskabsmænd og opfi
Gymnasieelever udvikler et billigt filter til at fjerne bly fra postevandetGymnasieelever udviklede et filter (hvis indersiden er vist her), der fastgøres til en vandhane og fjerner bly fra postevandet. Kredit:Rebecca Bushway Den næste generation af videnskabsmænd og opfi -
 Forsvindende handling:Enheden forsvinder på kommando efter militære missionerEn polymer (venstre) depolymeriserer og forsvinder efter at have været udsat for sollys i 10 minutter (højre). Kredit:Paul Kohl En polymer, der selvdestruerer? Mens engang en fiktiv idé, Der finde
Forsvindende handling:Enheden forsvinder på kommando efter militære missionerEn polymer (venstre) depolymeriserer og forsvinder efter at have været udsat for sollys i 10 minutter (højre). Kredit:Paul Kohl En polymer, der selvdestruerer? Mens engang en fiktiv idé, Der finde
- Hvorfor betragtes dværgplaneter på trods af at være mindre end nogle måner?
- Hvad er to af de længste floder i Frankrig?
- Verdensomspændende forringelse af jord og natur truer velstand og velvære
- Nutty Putty Cave:Før og efter 2009-tragedien
- reaktionen i en røgdetektor?
- Hvad er et materiale, der ikke har nogen elektrisk modstand?


