Smeltningspunktet for beryllium er 1287 C, mens den lithium 180 Hvad den store forskel i værdier?
* Metallisk binding: Både beryllium og lithium er metaller og udviser metallisk binding. Imidlertid påvirkes styrken af metallisk binding af faktorer som:
* atomstørrelse: Beryllium har en meget mindre atomradius end lithium. Dette betyder, at elektronerne i beryllium holdes tættere af kernen, hvilket resulterer i stærkere metallisk binding.
* Elektronkonfiguration: Beryllium har et højere antal valenselektroner end lithium. Disse elektroner bidrager til stærkere metallisk binding.
* krystalstruktur: Beryllium har en hexagonal tætpakket krystalstruktur, som er tættere og mere stabil end den kropscentrerede kubiske struktur af lithium. Denne strukturelle forskel bidrager yderligere til det højere smeltepunkt for beryllium.
Kortfattet:
Berylliums mindre størrelse, større antal valenselektroner og tættere krystalstruktur fører til stærkere metallisk binding, hvilket resulterer i et signifikant højere smeltepunkt sammenlignet med lithium.
Sidste artikelHvad er 50 procent svovl og ilt?
Næste artikelHvilke to faktorer fremskynder hastighederne for kemisk reaktion og forvitring?
 Varme artikler
Varme artikler
-
 Spilde bønnerne på kaffens sande identitetKredit:Pixabay/CC0 Public Domain Folk verden over ønsker, at deres kaffe både er tilfredsstillende og til en rimelig pris. For at opfylde disse standarder, ristemaskiner bruger typisk en blanding
Spilde bønnerne på kaffens sande identitetKredit:Pixabay/CC0 Public Domain Folk verden over ønsker, at deres kaffe både er tilfredsstillende og til en rimelig pris. For at opfylde disse standarder, ristemaskiner bruger typisk en blanding -
 Bioplast i bæredygtighedsdilemmaetTil dyrkning af sukkerrør, naturlig vegetation omdannes ofte til landbrugsjord og skove fældes. Kredit:OLOURBOX.de Plast fremstillet af afgrøder som majs eller sukkerrør i stedet for fossile brænd
Bioplast i bæredygtighedsdilemmaetTil dyrkning af sukkerrør, naturlig vegetation omdannes ofte til landbrugsjord og skove fældes. Kredit:OLOURBOX.de Plast fremstillet af afgrøder som majs eller sukkerrør i stedet for fossile brænd -
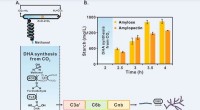 Kinesiske videnskabsmænd rapporterer om stivelsesyntese fra kuldioxidStivelsessyntese via kunstig stivelse anabolsk vej (ASAP) fra kuldioxid. Kredit:TIBCAS Kinesiske videnskabsmænd rapporterede for nylig om en de novo-rute til kunstig stivelsessyntese fra kuldioxid
Kinesiske videnskabsmænd rapporterer om stivelsesyntese fra kuldioxidStivelsessyntese via kunstig stivelse anabolsk vej (ASAP) fra kuldioxid. Kredit:TIBCAS Kinesiske videnskabsmænd rapporterede for nylig om en de novo-rute til kunstig stivelsessyntese fra kuldioxid -
 Udvikling af et bredt temperaturområde og højspændingsvandige MXene plane mikro-superkondensatore…(a) Det elektrokemiske stabilitetsvindue for højkoncentreret LiCl-vandig elektrolyt udvider sig til ~ 2,7 V. (b) Spændingsvinduet for MXene-elektrode i højkoncentreret LiCl-vandig elektrolyt udvides t
Udvikling af et bredt temperaturområde og højspændingsvandige MXene plane mikro-superkondensatore…(a) Det elektrokemiske stabilitetsvindue for højkoncentreret LiCl-vandig elektrolyt udvider sig til ~ 2,7 V. (b) Spændingsvinduet for MXene-elektrode i højkoncentreret LiCl-vandig elektrolyt udvides t
- Sammensætning af multikomponentlegeringer ved screening med høj gennemstrømning
- Hvad gør Superalloys Super:Hierarkisk mikrostruktur af en superlegering
- Almindelig ingrediens i husholdningsprodukter kan bidrage til antibiotikaresistens
- Ny undersøgelse afslører carbon nanorør måling mulig for første gang
- Hvordan Comcast forsøger at ændre kabelspillet
- Kasseret serviet hjælper amerikansk politi med at opklare en 32-årig mordgåde


