Hvad er den molekylære formel for et molekyle, der har en Ampirisk NH2 og molmasse 32G mol?
1. Find den empiriske formelmasse:
* N (nitrogen) har en molmasse på 14 g/mol
* H (brint) har en molmasse på 1 g/mol
* Den empiriske formel NH2 har en masse på 14 + (2 * 1) =16 g/mol
2. Beregn forholdet mellem molmasse og empirisk formelmasse:
* 32 g/mol (molmasse)/16 g/mol (empirisk formelmasse) =2
3. Multiplicer den empiriske formel -underskrifter med forholdet:
* NH2 * 2 = N2H4
Derfor er molekylets molekylære formel N2H4 (hydrazin).
Sidste artikelHvad er carbon tertra chlorid, og hvor bruger du dette?
Næste artikelHvad er sur klippe?
 Varme artikler
Varme artikler
-
 Surrey bygger AI til at finde kemiske forbindelser mod ældningKredit:CC0 Public Domain University of Surrey har opbygget en kunstig intelligens (AI) model, der identificerer kemiske forbindelser, der fremmer sund aldring - og baner vejen mod farmaceutiske in
Surrey bygger AI til at finde kemiske forbindelser mod ældningKredit:CC0 Public Domain University of Surrey har opbygget en kunstig intelligens (AI) model, der identificerer kemiske forbindelser, der fremmer sund aldring - og baner vejen mod farmaceutiske in -
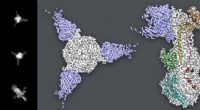 Cryo-EM-undersøgelse giver nye spor til skoldkopperinfektionBilleder ekstraheret fra cryo-EM-data (venstre og højre panel) viser varicella zoster-virusets gB-protein med tre antistoffer vedhæftet i enderne. Forskellige visninger af proteinet og antistoffer til
Cryo-EM-undersøgelse giver nye spor til skoldkopperinfektionBilleder ekstraheret fra cryo-EM-data (venstre og højre panel) viser varicella zoster-virusets gB-protein med tre antistoffer vedhæftet i enderne. Forskellige visninger af proteinet og antistoffer til -
 Nyudviklet COVID-19-test registrerer og identificerer specifikke varianter med 100 % nøjagtighedKredit:Unsplash/CC0 Public Domain University of California, Irvine forskere har udviklet en COVID-19-test, der detekterer og identificerer specifikke SARS-CoV-2-varianter med 100 % nøjagtighed. I e
Nyudviklet COVID-19-test registrerer og identificerer specifikke varianter med 100 % nøjagtighedKredit:Unsplash/CC0 Public Domain University of California, Irvine forskere har udviklet en COVID-19-test, der detekterer og identificerer specifikke SARS-CoV-2-varianter med 100 % nøjagtighed. I e -
 Discovery åbner nye veje til at designe lægemidler til at bekæmpe lægemiddelresistent malariaKredit:CC0 Public Domain For første gang, UBC-forskere har vist en nøgleforskel i de tredimensionelle strukturer af et centralt metabolisk enzym i parasitten, der forårsager malaria sammenlignet m
Discovery åbner nye veje til at designe lægemidler til at bekæmpe lægemiddelresistent malariaKredit:CC0 Public Domain For første gang, UBC-forskere har vist en nøgleforskel i de tredimensionelle strukturer af et centralt metabolisk enzym i parasitten, der forårsager malaria sammenlignet m
- Hvad er de 3 hovedtyper af energi, som Sun udsender?
- Undersøgelse afslører radikale rynker i dannelsen af komplekse kulstofmolekyler i rummet
- Hvad er nogle problemer med forgasningsprocessen?
- Hvad er de 16 forskellige organismer, der repræsenterer evolution fra celle til menneske?
- Hvad er mediet for bølger på en forår?
- Hvilken type homeostatiske mekanismer er indbygget i organerne, der reguleres?


