Hvad er de kemiske egenskaber ved brint?
Kemiske egenskaber ved brint:
Hydrogen, det enkleste element med kun en proton og en elektron, udviser unikke kemiske egenskaber på grund af dets lille størrelse og tilstedeværelsen af kun et elektron i dets yderste skal. Her er nogle af de vigtigste egenskaber:
1. Reaktivitet:
* Meget reaktiv: Brint er meget reaktivt og danner let kemiske bindinger med andre elementer. Dette skyldes dets høje elektronegativitet og dens evne til at deltage i både ionisk og kovalent binding.
* kombineres med ikke -metaller: Den danner let forbindelser med ikke -metaller som ilt (vand), klor (hydrogenchlorid) og nitrogen (ammoniak).
* kombineres med metaller: Hydrogen kan også danne forbindelser med metaller, danner hydrider som natriumhydrid (NAH).
2. Oxidation siger:
* +1: Den mest almindelige oxidationstilstand for brint er +1, især når det binder sig med ikke -metaller.
* -1: Hydrogen kan også eksistere i en -1 -oxidationstilstand, især når det bindinger med metaller.
3. Binding:
* kovalent binding: Hydrogen danner stærke kovalente bindinger med ikke -metaller, der deler elektroner for at opnå en stabil konfiguration.
* ionisk binding: Det kan også deltage i ionisk binding med stærkt elektropositive metaller og danne hydrider.
* Hydrogenbinding: Hydrogen kan danne svage brintbindinger med elektronegative elementer som ilt, nitrogen og fluor, der spiller en afgørende rolle i egenskaberne ved vand og andre molekyler.
4. Forbrænding:
* brandfarlig: Brintgas er meget brandfarlig og forbrænder med en lyseblå flamme.
* producerer vand: Ved forbrænding reagerer brint med ilt for at producere vand og frigiver en betydelig mængde varmeenergi.
* Brugt som brændstof: På grund af sin høje energitæthed og rene forbrændingsprodukter (vand) betragtes brint som et lovende fremtidig brændstof.
5. Isotoper:
* Protium (¹H): Den mest almindelige isotop af brint med en proton og ingen neutroner.
* deuterium (²h): Indeholder en proton og en neutron.
* tritium (³h): Indeholder en proton og to neutroner.
6. Andre egenskaber:
* farveløs, lugtfri og smagløs: Brintgas er farveløs, lugtfri og smagløs i sin rene form.
* letteste element: Hydrogen er det letteste element med en atommasse på cirka 1 atommasseenhed (AMU).
* rigeligt element: Hydrogen er det mest rigelige element i universet, der udgør cirka 75% af dets masse.
Ansøgninger:
Hydrogen har en bred vifte af applikationer, herunder:
* brændstof: Brugt som brændstof i forskellige applikationer, herunder brændselsceller og forbrændingsmotorer.
* Produktion af ammoniak: Brugt til produktion af ammoniak, en nøgleingrediens til gødning og andre industriprodukter.
* Kemisk syntese: Brugt som et reduktionsmiddel i forskellige kemiske reaktioner, herunder produktion af methanol og andre kemikalier.
* Fødevarebehandling: Bruges til at hydrogenere vegetabilske olier og omdanne dem til faste fedtstoffer.
At forstå disse kemiske egenskaber er afgørende for at værdsætte alsidigheden og betydningen af brint på forskellige felter.
Sidste artikelHvad er formlen for anionchlorid?
Næste artikelHvilken farve er natriumsulfit i vand?
 Varme artikler
Varme artikler
-
 Forskere udvikler genbrug til kulfiberkompositterWashington State University professor Jinwen Zhang med sit forskergruppe for genbrug af kulfiber. Kredit:Washington State University Et WSU -forskerhold har for første gang udviklet en lovende måd
Forskere udvikler genbrug til kulfiberkompositterWashington State University professor Jinwen Zhang med sit forskergruppe for genbrug af kulfiber. Kredit:Washington State University Et WSU -forskerhold har for første gang udviklet en lovende måd -
 Forskere laver bæredygtig polymer af sukkerarter i træDen nye polymer er fremstillet ved hjælp af xylose, et sukker, der findes i træ. Kredit:Leszek Kobusinski Forskere fra University of Bath har lavet en bæredygtig polymer ved at bruge det næstmest
Forskere laver bæredygtig polymer af sukkerarter i træDen nye polymer er fremstillet ved hjælp af xylose, et sukker, der findes i træ. Kredit:Leszek Kobusinski Forskere fra University of Bath har lavet en bæredygtig polymer ved at bruge det næstmest -
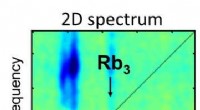 Forskere anvender 2-D spektroskopi til isolerede molekylære systemer for første gang2-D spektroskopi illustrerer de lysinducerede reaktioner af Rubidium molekyler i forskellige farvespektre. Illustration:Lukas Bruder Et forskerhold ledet af Prof. Dr. Frank Stienkemeier og Dr. Luk
Forskere anvender 2-D spektroskopi til isolerede molekylære systemer for første gang2-D spektroskopi illustrerer de lysinducerede reaktioner af Rubidium molekyler i forskellige farvespektre. Illustration:Lukas Bruder Et forskerhold ledet af Prof. Dr. Frank Stienkemeier og Dr. Luk -
 Nye mælkesyrebakterier skaber naturlig sødme i yoghurtKredit:Pixabay/CC0 Public Domain Forskere på DTU har udviklet en yoghurtbakterie, som kan spalte laktose på en omkostningseffektiv og bæredygtig måde. Dette gør det muligt at skabe naturlig sødme i
Nye mælkesyrebakterier skaber naturlig sødme i yoghurtKredit:Pixabay/CC0 Public Domain Forskere på DTU har udviklet en yoghurtbakterie, som kan spalte laktose på en omkostningseffektiv og bæredygtig måde. Dette gør det muligt at skabe naturlig sødme i
- Revolveres jorden om solen i en perfekt cirkel?
- En elektrolytdrik med kyllingesmag kunne hjælpe snifferhunde med at forblive hydrerede
- Er varme produceret af nuklear fusion får stjerner til at gløde sandt eller falsk?
- Lav opadgående mobilitet forbundet med tidlig dødelighed
- En ny tilgang til at opdage visuelle mønstre i kunstsamlinger
- Nanotekniske narkotikasmuglere


