Hvordan dannes natriumzinkat?
Sådan dannes det i løsning:
1. Reaktion af zinkoxid med natriumhydroxid:
* Når zinkoxid (ZnO) reagerer med en koncentreret opløsning af natriumhydroxid (NaOH), opstår der en kompleks reaktion, hvor zinkationer ([ZnO₂] ²⁻) dannes.
Ligning:
Zno (S) + 2NAOH (aq) → Na₂zno₂ (aq) + h₂o (l)
* Denne reaktion er reversibel, og dannelsen af natriumzinkat favoriseres i en høj koncentration af hydroxidioner.
2. Elektroplettering af zink:
* I elektropletteringsprocessen deponeres zinkmetal på en metaloverflade. Denne proces involverer typisk en opløsning, der indeholder zinkioner (Zn²⁺) og natriumhydroxid (NaOH).
* Under elektroplettering reagerer hydroxidioner (OH⁻) med zinkioner for at danne zinkhydroxid (Zn (OH) ₂) som et mellemprodukt.
Ligning:
Zn²⁺ (aq) + 2OH⁻ (aq) → Zn (OH) ₂ (s)
* Zinkhydroxid reagerer yderligere med overskydende hydroxidioner for at danne zinkationer.
Ligning:
Zn (OH) ₂ (S) + 2OH⁻ (aq) → [Zno₂] ²⁻ (aq) + 2H₂O (L)
* Zinkationer migrerer derefter til katoden (negativ elektrode) og reduceres til zinkmetal, der aflejres på overfladen.
Vigtig note:
* Natriumzinkat er en hypotetisk forbindelse, og det findes kun i opløsning som en kompleks ion. Dens stabilitet er meget afhængig af opløsningsbetingelserne, herunder pH og koncentration.
* Den nøjagtige kemiske struktur af zinkationer i opløsning er stadig et spørgsmål om debat og kan variere afhængigt af reaktionsbetingelserne.
Selvom natriumzinket ikke er et stabilt fast stof, er det et vigtigt mellemprodukt i forskellige reaktioner, især i elektropletteringsprocessen.
Sidste artikelHvad er den kemiske formel for molybdænacetat?
Næste artikelHvad er vismuthchlorid i?
 Varme artikler
Varme artikler
-
 Undersøgelse undersøger kemikaliet GenX i vand:Er det forskelligt fra andre PFAS?Fotoillustrationen viser GenX-molekyler, de røde og grønne cirkler, overlejret over en strøm. samspillet mellem GenX og vand fører til dannelsen af miceller, som forekommer i højere koncentrationer
Undersøgelse undersøger kemikaliet GenX i vand:Er det forskelligt fra andre PFAS?Fotoillustrationen viser GenX-molekyler, de røde og grønne cirkler, overlejret over en strøm. samspillet mellem GenX og vand fører til dannelsen af miceller, som forekommer i højere koncentrationer -
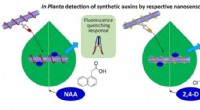 Forskere designer sensorer til hurtigt at opdage plantehormonerNanosensorer udviklet ved Singapore-MIT Alliance for Research and Technology (SMART) kan detektere syntetiske auxin plantehormoner NAA og 2, 4-D. Kredit:Singapore-MIT Alliance for Research and Technol
Forskere designer sensorer til hurtigt at opdage plantehormonerNanosensorer udviklet ved Singapore-MIT Alliance for Research and Technology (SMART) kan detektere syntetiske auxin plantehormoner NAA og 2, 4-D. Kredit:Singapore-MIT Alliance for Research and Technol -
 Tekstil-baserede kompositter kan væve fremtiden for rumfartsteknikFlettemaskine. Kredit:University of Manchester Avanceret materialeforskning ved University of Manchester har vist et omfattende billede af udviklingen af skader i flettede tekstilkompositter for
Tekstil-baserede kompositter kan væve fremtiden for rumfartsteknikFlettemaskine. Kredit:University of Manchester Avanceret materialeforskning ved University of Manchester har vist et omfattende billede af udviklingen af skader i flettede tekstilkompositter for -
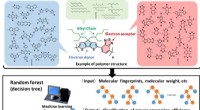 AI-software hjælper med design af nyt materiale til solcellerFig. 1. Udforskning af nye polymerer til polymersolceller ved hjælp af materialeinformatik. (Øvre) Eksempel på en polymerstruktur bestående af elektrondonor, elektronacceptor, og alkylkæder. (Mellem)
AI-software hjælper med design af nyt materiale til solcellerFig. 1. Udforskning af nye polymerer til polymersolceller ved hjælp af materialeinformatik. (Øvre) Eksempel på en polymerstruktur bestående af elektrondonor, elektronacceptor, og alkylkæder. (Mellem)
- Solpanelets udgangsvande
- Simuleringseksperiment tillader dybere indsigt i ultrahurtige lysinducerede processer
- Hvad er den største af jordbaserede planeter i solsystemet?
- Dyre- og plantelivscykler
- En ny salvinia-lignende glat overflade
- Australske landmænd ønsker mere klimaindsats, og de starter i deres egne (store) baghaver


