Hvordan nedbryder du den sammensatte P4CL10?
Her er den afbalancerede kemiske ligning:
P4CL10 + 8 H2O → 4 H3PO4 + 10 HCI
Forklaring:
* p4cl10: Dette er phosphor (V) chlorid, også kendt som fosforpentachlorid. Det er en meget reaktiv forbindelse.
* H2O: Vand er den reaktant, der forårsager nedbrydningen.
* H3PO4: Fosforsyre dannes som et produkt af reaktionen. Det er en svag syre, der ofte bruges i gødning og fødevaretilsætningsstoffer.
* hcl: Hydrogenchlorid er et andet produkt. Det er en stærk syre, der opløses i vand til dannelse af saltsyre.
Reaktionsdetaljer:
Reaktionen er eksoterm, hvilket betyder, at den frigiver varme. Fosfor- og kloratomerne i P4CL10 er meget elektronegative, hvilket gør molekylet ustabile. Når der tilsættes vand, angriber iltatomerne i vand fosforatomerne, bryder P-CL-bindingerne og danner P-O-bindinger. Dette resulterer i dannelsen af fosforsyre og hydrogenchlorid.
Sikkerhedsforholdsregler:
* P4CL10 er en meget ætsende og giftig forbindelse. Det skal håndteres med omhu i et godt ventileret område.
* Reaktionen producerer ætsende dampe af HCL. Det er vigtigt at bære passende sikkerhedsudstyr, herunder handsker, beskyttelsesbriller og en åndedrætsværn, når man arbejder med denne forbindelse.
Bemærk: Mens vand er den mest almindelige måde at nedbryde P4CL10 på, er andre reaktioner mulige. For eksempel kan P4CL10 også reagere med alkoholer til dannelse af estere.
Sidste artikelHvad er valensen af brintsulfat?
Næste artikelHvad sker der, når kobbersulfat og natriumhydroxid opvarmes?
 Varme artikler
Varme artikler
-
 En bioplast, der beskytter mod UV-strålingKredit:Oulu Universitet Forskere ved Uleåborgs universitets forskningsenhed for bæredygtig kemi har udviklet en ny syntetisk bioplast, der i modsætning til traditionel kulstofbaseret plast eller a
En bioplast, der beskytter mod UV-strålingKredit:Oulu Universitet Forskere ved Uleåborgs universitets forskningsenhed for bæredygtig kemi har udviklet en ny syntetisk bioplast, der i modsætning til traditionel kulstofbaseret plast eller a -
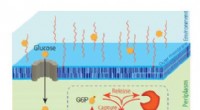 Opdagelse af nyt fænomen en game-changer for effektiv bioproduktion af nyttige kemikalierG6P-sekretionsmekanismen opdaget i denne undersøgelse. Kredit:Kobe University Et forskningssamarbejde har opdaget en ny mekanisme, hvorved glukose, der blev fanget af E. coli, derefter udskilles fr
Opdagelse af nyt fænomen en game-changer for effektiv bioproduktion af nyttige kemikalierG6P-sekretionsmekanismen opdaget i denne undersøgelse. Kredit:Kobe University Et forskningssamarbejde har opdaget en ny mekanisme, hvorved glukose, der blev fanget af E. coli, derefter udskilles fr -
 Akustisk mikrofluidisk platform adskiller forsigtigt og hurtigt cirkulerende tumorceller fra blodprø…Ved hjælp af lydbølger, et internationalt forskerteam har udviklet en blid, kontaktfri metode til adskillelse af cirkulerende tumorceller fra blodprøver, der er hurtig og effektiv nok til klinisk brug
Akustisk mikrofluidisk platform adskiller forsigtigt og hurtigt cirkulerende tumorceller fra blodprø…Ved hjælp af lydbølger, et internationalt forskerteam har udviklet en blid, kontaktfri metode til adskillelse af cirkulerende tumorceller fra blodprøver, der er hurtig og effektiv nok til klinisk brug -
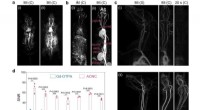 En simpel opskrift på MR-kontraster er op til fire gange højereIn vivo MR angiografi. a, b Kontrastforstærket MR-angiografi (MRA) billeder af hele kroppen på en rotte og b kanin umiddelbart efter bolusinjektionen af (i) Gd-DTPA og (ii) ACNC. c MRA-billeder af o
En simpel opskrift på MR-kontraster er op til fire gange højereIn vivo MR angiografi. a, b Kontrastforstærket MR-angiografi (MRA) billeder af hele kroppen på en rotte og b kanin umiddelbart efter bolusinjektionen af (i) Gd-DTPA og (ii) ACNC. c MRA-billeder af o
- Hvad kaldes en bakke med stejl side?
- Er den akademiske verden blevet mere kønsretfærdig for kvinder? Resultater fra en kontradiktorisk …
- Lavenergi-Iris forventes ikke at have stor indflydelse
- Hvor mange solcellepaneler er der på den internationale rumstation?
- Hvilket udtryk bruges til at beskrive en repræsentation af ting eller system og kan være som en må…
- Hvordan kan du beskrive en gas?


