Hvilket element har egenskaber, der ligner klor og fluor?
Her er hvorfor:
* halogener: Alle tre elementer (klor, fluor og brom) hører til gruppe 17 i den periodiske tabel, kendt som halogenerne.
* Lignende reaktivitet: Halogener er meget reaktive ikke -metaller. De har en tendens til at få en elektron for at opnå en stabil elektronkonfiguration.
* Lignende kemiske egenskaber: Alle tre danner diatomiske molekyler (CL2, F2, BR2) og deler lignende reaktivitetsmønstre i dannelse af forbindelser.
Nøgleforskelle:
Mens de er lignende, har de forskelle:
* Elektronegativitet: Fluor er det mest elektronegative element, efterfulgt af klor, derefter brom.
* kogepunkter: Brom er en væske ved stuetemperatur, mens klor er en gas og fluor er en gas.
* reaktivitet: Fluor er den mest reaktive halogen, efterfulgt af klor, derefter brom.
Fortæl mig, hvis du har andre spørgsmål!
Sidste artikelHvordan kan kogepunktet for et kemikalie fortælle dig, hvor ren det er?
Næste artikelEr brom et fast stof ved stuetemperatur?
 Varme artikler
Varme artikler
-
 Polymerer bliver fanget af kærlighed-hadkemi af olie og vandForskere ved Oak Ridge National Laboratory og University of Tennessee sporede polymerselvsamling ved væske-væske-grænsefladen i realtid. Kredit:Michelle Lehman/Oak Ridge National Laboratory, US Depart
Polymerer bliver fanget af kærlighed-hadkemi af olie og vandForskere ved Oak Ridge National Laboratory og University of Tennessee sporede polymerselvsamling ved væske-væske-grænsefladen i realtid. Kredit:Michelle Lehman/Oak Ridge National Laboratory, US Depart -
 Alternative cementopskrifter - En opskrift på øko-betonIngredienserne til øko-cement blandes i betonlaboratoriet. Kredit:Empa Det er det mest udbredte produkt i verden. Cement er uundværlig, men dets omdømme er blevet ret plettet i løbet af den igangv
Alternative cementopskrifter - En opskrift på øko-betonIngredienserne til øko-cement blandes i betonlaboratoriet. Kredit:Empa Det er det mest udbredte produkt i verden. Cement er uundværlig, men dets omdømme er blevet ret plettet i løbet af den igangv -
 Forbedring af genleveringsmetoderKredit:Royal Society of Chemistry Forskere i Kina undersøger nye måder at behandle kræft på ved hjælp af genterapi. Vi finder ud af, hvordan deres arbejde inspirerede dette smukke og indviklede de
Forbedring af genleveringsmetoderKredit:Royal Society of Chemistry Forskere i Kina undersøger nye måder at behandle kræft på ved hjælp af genterapi. Vi finder ud af, hvordan deres arbejde inspirerede dette smukke og indviklede de -
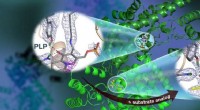 Neutroner observerer vitamin B6-afhængig enzymaktivitet, der er nyttig til lægemiddeludviklingEt ORNL-ledet team brugte neutroner til at observere AAT-enzymet, et vitamin B6-afhængigt protein, og fandt ud af, at den kemiske reaktion kun fandt sted på ét aktivt sted. Nuklear spredningslængde tæ
Neutroner observerer vitamin B6-afhængig enzymaktivitet, der er nyttig til lægemiddeludviklingEt ORNL-ledet team brugte neutroner til at observere AAT-enzymet, et vitamin B6-afhængigt protein, og fandt ud af, at den kemiske reaktion kun fandt sted på ét aktivt sted. Nuklear spredningslængde tæ


