Hvordan konverteres jernoxid til metal?
Her er en sammenbrud af processen:
1. Minedrift og forberedelse:
* Jernmalm, der indeholder jernoxid, udvindes.
* Malmen er knust og malet for at øge overfladearealet for bedre reaktion.
2. Smeltning:
* Den knuste malm blandes med cokke (Carbon) og kalksten (calciumcarbonat) og placeret i en blastovn .
* Varm luft sprænges i ovnen, hvilket får koks til at brænde, generere varme og kulilte (CO).
* Kemiske reaktioner:
* reduktion: Kulmonoxid reagerer med jernoxidet for at danne jern- og kuldioxid (CO₂):
* fe₂o₃ + 3co → 2fe + 3co₂
* Kalksten nedbrydning: Kalksten nedbrydes til calciumoxid (CAO) og kuldioxid:
* caco₃ → Cao + co₂
* Slagdannelse: Calciumoxid reagerer med urenheder i malmen og danner slagge , som er et smeltet affaldsprodukt:
* Cao + SiO₂ → Casio₃ (slagge)
3. Raffinering og casting:
* Det smeltede jern opsamles i bunden af højovnen.
* Slaggen er skummet fra overfladen.
* Jernet raffineres yderligere for at fjerne urenheder og kastes derefter i forskellige former.
Samlede reaktioner:
Hele processen kan repræsenteres ved følgende forenklede ligning:
fe₂o₃ + 3c → 2fe + 3co
Nøglepunkter:
* carbonmonoxid (CO) er det primære reduktionsmiddel i denne proces.
* koks Tilvejebringer kulstofkilden til reaktionen.
* kalksten bruges til at fjerne urenheder og danne slagge.
* smeltning er en høj temperaturproces, der kræver meget energi.
* Det resulterende jern er ikke 100% rent og kan indeholde urenheder.
Andre metoder:
Mens højovn er den mest almindelige metode, kan andre teknikker bruges til at omdanne jernoxid til jern, såsom:
* Direkte reduktion: Dette bruger naturgas til at reducere jernoxid ved lavere temperaturer.
* elektrolyse: Dette bruger elektricitet til at reducere jernoxid, men er generelt dyrere.
Valget af metode afhænger af faktorer som typen af jernoxid, den ønskede renhed af jernet og produktionsomkostningerne.
Sidste artikelHvad er formlen for Mercury II -oxid?
Næste artikelEr brændende brint en kemisk egenskab?
 Varme artikler
Varme artikler
-
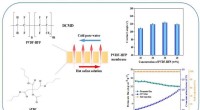 En lovende løsning til at forbedre overfladehydrofobiciteten af hydrofobe membranerKredit:Jun Pan et al., Grænser for kemividenskab og ingeniørvidenskab (2022) Som mange kemikere ved, har membrandestillation (MD) processen vundet stigende popularitet og opmærksomhed for saltvands
En lovende løsning til at forbedre overfladehydrofobiciteten af hydrofobe membranerKredit:Jun Pan et al., Grænser for kemividenskab og ingeniørvidenskab (2022) Som mange kemikere ved, har membrandestillation (MD) processen vundet stigende popularitet og opmærksomhed for saltvands -
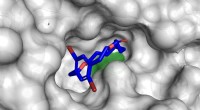 At forme molekylernes ringeModel chiral makrocyklus (vist i blåt) i den katalytiske lomme af enzymet CALB (vist i gråt, katalytisk serin 105 farvet i grøn [PDB ID 5GV5]). Figuren blev genereret ved hjælp af PyMOL Molecular Grap
At forme molekylernes ringeModel chiral makrocyklus (vist i blåt) i den katalytiske lomme af enzymet CALB (vist i gråt, katalytisk serin 105 farvet i grøn [PDB ID 5GV5]). Figuren blev genereret ved hjælp af PyMOL Molecular Grap -
 Enkelt molekyle kontrol i en milliontedel af en milliardtedel af et sekundScanning Tunneling Mikroskop. Kredit:University of Bath Fysikere ved University of Bath har opdaget, hvordan man manipulerer og kontrollerer individuelle molekyler i en milliontedel af en milliard
Enkelt molekyle kontrol i en milliontedel af en milliardtedel af et sekundScanning Tunneling Mikroskop. Kredit:University of Bath Fysikere ved University of Bath har opdaget, hvordan man manipulerer og kontrollerer individuelle molekyler i en milliontedel af en milliard -
 En ny gelelektroforese teknik til hurtig biomarkørdiagnose via massespektrometriOpløselige BAC-tværbundne geler muliggør hurtig og tabsfri genvinding af proteinbiomarkører adskilt af SDS-polyacrylamidgelelektroforese og letter analyse ved massespektrometri. Kredit: Journal of Pro
En ny gelelektroforese teknik til hurtig biomarkørdiagnose via massespektrometriOpløselige BAC-tværbundne geler muliggør hurtig og tabsfri genvinding af proteinbiomarkører adskilt af SDS-polyacrylamidgelelektroforese og letter analyse ved massespektrometri. Kredit: Journal of Pro
- Hvorfor er det vanskeligt for forskere at observere planeter i rummet ud over solsystemet?
- Vold mod kvinder i videospillet Red Dead Redemption 2 fremkalder giftig maskulinitet
- Hvad er de forskellige typer af vandlegemer som havsø osv.?
- Forskere, der udforsker spintronik i grafen
- Sådan beregnes maksimal belastningsbelastning
- Isolerede stammemedlemmer i Brasilien opdaget i droneoptagelser


