Reaktion mellem kaliumdichromat og jernsulfat?
reaktionen:
K₂cr₂o₇ (aq) + 6feso₄ (aq) + 7H₂so₄ (aq) → cr₂ (so₄) ₃ (aq) + 3fe₂ (so₄) ₃ (aq) + k₂so₄ (aq) + 7h₂o (l)
Forklaring:
* redox -proces: Kaliumdichromat fungerer som et oxidationsmiddel og bliver reduceret til krom (III) sulfat (Cr₂ (SO₄) ₃). Jern (II) sulfat fungerer som et reduktionsmiddel og bliver oxideret til jern (III) sulfat (Fe₂ (SO₄) ₃).
* Betingelser: Denne reaktion forekommer typisk under sure forhold. Svovlsyre (H₂so₄) tilvejebringer det nødvendige sure miljø.
* Produkter:
* Chromium (III) sulfat (Cr₂ (SO₄) ₃) - En grøn opløsning
* Jern (III) sulfat (Fe₂ (SO₄) ₃) - En gul opløsning
* Kaliumsulfat (k₂so₄) - forbliver i opløsning
* Vand (H₂O) - et biprodukt
Nøglepunkter:
* farveændring: Løsningen ændres fra en lysegrøn (på grund af fe²⁺-ioner) til en gulbrun farve (på grund af fe³⁺-ioner), når reaktionen skrider frem.
* afbalancering af ligningen: Ligningen skal omhyggeligt afbalanceres for at sikre, at antallet af atomer i hvert element er det samme på begge sider.
* applikationer: Denne reaktion bruges ofte i analytisk kemi til bestemmelse af jern (II) -ioner.
Sikkerhedsforholdsregler:
* Kaliumdichromat er et stærkt oxidationsmiddel og kan være giftigt. Håndter det med omhu og bære passende sikkerhedsudstyr.
* Undgå kontakt med hud, øjne og tøj.
* Arbejd altid i et godt ventileret område.
Fortæl mig, hvis du har yderligere spørgsmål om denne reaktion!
 Varme artikler
Varme artikler
-
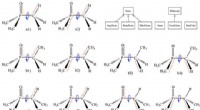 Forskere designer udvindingsmidler til sjældne jordarter ved hjælp af ny softwareKredit:Ames Laboratory U.S. Department of Energys Critical Materials Institute har udviklet et computerprogram, kaldet ParFit, som i høj grad kan reducere mængden af tid brugt på at identificere
Forskere designer udvindingsmidler til sjældne jordarter ved hjælp af ny softwareKredit:Ames Laboratory U.S. Department of Energys Critical Materials Institute har udviklet et computerprogram, kaldet ParFit, som i høj grad kan reducere mængden af tid brugt på at identificere -
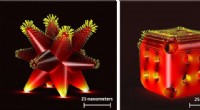 Metalkatalysatorer, der bruges til miljømæssig bæredygtighed, viste sig at nedbrydes og blive min…Nogle af de komplekse strukturelle arrangementer af katalysatorer; venstre er kendt som forgrenet struktur og højre som burstruktur. Kredit:Professor Anna Klinkova fra University of Waterloo Ny fo
Metalkatalysatorer, der bruges til miljømæssig bæredygtighed, viste sig at nedbrydes og blive min…Nogle af de komplekse strukturelle arrangementer af katalysatorer; venstre er kendt som forgrenet struktur og højre som burstruktur. Kredit:Professor Anna Klinkova fra University of Waterloo Ny fo -
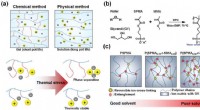 Et termometer, der kan strækkes og deformeres af vandVirkningerne af ionisk sidekæde. a) Skema, der angiver forskel med hensyn til brugstid og termisk stabilitet i henhold til kemiske og fysiske metoder. b) Skema for P(SPMA-r-MMA)er og vandopløselighed.
Et termometer, der kan strækkes og deformeres af vandVirkningerne af ionisk sidekæde. a) Skema, der angiver forskel med hensyn til brugstid og termisk stabilitet i henhold til kemiske og fysiske metoder. b) Skema for P(SPMA-r-MMA)er og vandopløselighed. -
 Nyheder om bæredygtig plante-afledt plast til at hjælpe organforskningDr. Maïwenn Kersaudy-Kerhoas og Alfredo Ongaro arbejder i laboratoriet med PLA. Kredit:Heriot-Watt University Dr. Maïwenn Kersaudy-Kerhoas og Alfredo Ongaro fra Institute of Biological Chemistry,
Nyheder om bæredygtig plante-afledt plast til at hjælpe organforskningDr. Maïwenn Kersaudy-Kerhoas og Alfredo Ongaro arbejder i laboratoriet med PLA. Kredit:Heriot-Watt University Dr. Maïwenn Kersaudy-Kerhoas og Alfredo Ongaro fra Institute of Biological Chemistry,
- Det er tid til at begynde at tænke på vores digitale kulstofaftryk
- Træ eller stor busk med afrundede blade og spiselige brune nødder?
- Hvorfor skal antallet af atomer hvert element forblive det samme i en kemisk ligning?
- Hvordan man tackler ekstremisme blandt unge og radikaliserede
- To piloter, raketforsker, oceanograf, der flyver SpaceX
- Hvad blandt skorpemantelen og kernen har den højeste tæthed?


