Vil cesiumchlorid opløses i vand?
Her er hvorfor:
* ionisk forbindelse: Cesiumchlorid er en ionisk forbindelse, hvilket betyder, at det dannes af den elektrostatiske tiltrækning mellem positivt ladede cæsiumioner (CS+) og negativt ladede chloridioner (Cl-).
* polært opløsningsmiddel: Vand er et polært opløsningsmiddel, hvilket betyder, at det har en positiv og negativ ende på grund af den ujævne deling af elektroner i molekylet. Dette gør det muligt for vandmolekyler at interagere med ionerne i CSCL.
* Hydrering: Når CSCL tilsættes til vand, omgiver vandmolekylerne ionerne, adskiller dem fra hinanden og opløses forbindelsen. Denne proces kaldes hydrering.
Det er dog vigtigt at bemærke, at:
* opløselighed: Mens CSCL opløses i vand, er dens opløselighed begrænset. Dette betyder, at kun en vis mængde CSCL kan opløses i en given mængde vand ved en bestemt temperatur.
* eksotermisk reaktion: Opløsningen af CSCL i vand er en eksoterm reaktion, hvilket betyder, at den frigiver varme.
Generelt er cæsiumchlorid opløseligt i vand på grund af dets ioniske natur og vandets evne til at hydratere ionerne.
 Varme artikler
Varme artikler
-
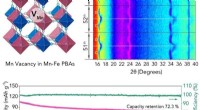 Forskning driver genopladelige batterier, der holder længereForskere udviklede et meget stabilt katodemateriale til natriumlagring. Kredit:SUTD Med den løbende forbedring af elektronik, udviklingen af højenergi-strømforsyninger er blevet et nøgleled i de
Forskning driver genopladelige batterier, der holder længereForskere udviklede et meget stabilt katodemateriale til natriumlagring. Kredit:SUTD Med den løbende forbedring af elektronik, udviklingen af højenergi-strømforsyninger er blevet et nøgleled i de -
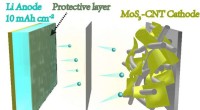 Kemikere finder en ny måde at skabe lithiummetalelektroder til batterierDette billede viser den skematiske struktur af en ny battericelle med lithiummetalelektroder udviklet ved Yale og Donghua University. Kredit:Yale University Forskere ved Yale og Donghua University
Kemikere finder en ny måde at skabe lithiummetalelektroder til batterierDette billede viser den skematiske struktur af en ny battericelle med lithiummetalelektroder udviklet ved Yale og Donghua University. Kredit:Yale University Forskere ved Yale og Donghua University -
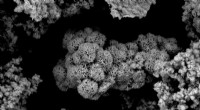 Klimabeskyttelse:CO2 omdannet til methanolMolybdændisulfid under scanningselektronmikroskopet. Kredit:Vienna University of Technology Af hensyn til klimabeskyttelsen må kuldioxid ikke frigives til atmosfæren. Hvor dannelsen af kuldioxid
Klimabeskyttelse:CO2 omdannet til methanolMolybdændisulfid under scanningselektronmikroskopet. Kredit:Vienna University of Technology Af hensyn til klimabeskyttelsen må kuldioxid ikke frigives til atmosfæren. Hvor dannelsen af kuldioxid -
 Afkodning af materialeslitage med supercomputereEt lille stykke metal simuleres på en computer - atom for atom. Kredit:TU Wien Slid og friktion er afgørende spørgsmål i mange industrisektorer:Hvad sker der, når en overflade glider hen over en a
Afkodning af materialeslitage med supercomputereEt lille stykke metal simuleres på en computer - atom for atom. Kredit:TU Wien Slid og friktion er afgørende spørgsmål i mange industrisektorer:Hvad sker der, når en overflade glider hen over en a
- Hvorfor ekstraheres zink ikke fra oxid gennem reduktion ved hjælp af kulilte?
- En kort definition til videnskabelig metode?
- Hvis det var 85 grader F ved jordoverfladen, hvad ville temperaturen der være på toppen af en 25…
- Amerikanske flyselskaber lander flere fly, efterhånden som rejsekrisen bliver dybere
- Hvorfor er den kemiske sammensætning af et mineral vigtig?
- Hvor mange blokke svarer til en kilometer i Olivia MN?


