Hvorfor er hydrogenchlorid god leder af elektricitet?
* kovalent binding: HCL findes som en gas ved stuetemperatur. Brint- og kloratomerne er bundet sammen kovalent og deler elektroner. Dette betyder, at der ikke er nogen frit bevægende ladede partikler (ioner) til at bære en elektrisk strøm.
Når HCL opløses i vand (danner saltsyre), bliver det imidlertid en fremragende leder af elektricitet :
* ionisering: HCL-molekyler reagerer med vand og bryder fra hinanden i hydrogenioner (H+) og chloridioner (Cl-):
`` `
HCl (G) + H2O (L) → H3O + (aq) + Cl- (aq)
`` `
* Gratis ioner: Tilstedeværelsen af disse frie ioner, der er ladede partikler, tillader elektricitet at strømme gennem opløsningen. De positivt ladede hydrogenioner bevæger sig mod den negative elektrode (katode), og de negativt ladede chloridioner bevæger sig mod den positive elektrode (anode).
Kortfattet:
* Gasformet HCL er en dårlig leder Fordi det mangler frie ioner.
* Vandig HCL (saltsyre) er en god leder Fordi det ioniserer, producerer de frie ioner, der bærer den elektriske strøm.
Sidste artikelVil cesiumchlorid opløses i vand?
Næste artikelHvad er den afbalancerede ligning for Mercury2 nitrat og natriumphosphat?
 Varme artikler
Varme artikler
-
 Forskere opdager en spænding, der afhænger af bølgelængden af indfaldende lysSbSI og SbSI:Sb2 S3 fotovoltaiske apparater. Kredit:Ryosuke Nishikubo Forskere fra Institute for Open and Transdisciplinary Research Initiatives ved Osaka University opdagede en ny funktion af solc
Forskere opdager en spænding, der afhænger af bølgelængden af indfaldende lysSbSI og SbSI:Sb2 S3 fotovoltaiske apparater. Kredit:Ryosuke Nishikubo Forskere fra Institute for Open and Transdisciplinary Research Initiatives ved Osaka University opdagede en ny funktion af solc -
 Undersøgelse af glødende glasdråber på ISSNul tyngdekraft:Forskere ved University of Ulm under en smeltetest i Zero-GAirbus fra virksomheden Novespace. Kredit:Airbus Defence and Space Forskere vil snart studere materialeprøver på ISS. De p
Undersøgelse af glødende glasdråber på ISSNul tyngdekraft:Forskere ved University of Ulm under en smeltetest i Zero-GAirbus fra virksomheden Novespace. Kredit:Airbus Defence and Space Forskere vil snart studere materialeprøver på ISS. De p -
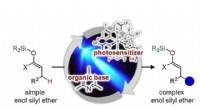 Muliggør selektiv carbon-carbon-bindingsdannelse i enolsilylethers iboende inaktive positionFigur:En ny transformation til effektiv syntese af komplekse organiske molekyler Nagoya University forskere har opdaget en ny måde at ændre reaktanter, der er blevet bredt undersøgt og anvendt i o
Muliggør selektiv carbon-carbon-bindingsdannelse i enolsilylethers iboende inaktive positionFigur:En ny transformation til effektiv syntese af komplekse organiske molekyler Nagoya University forskere har opdaget en ny måde at ændre reaktanter, der er blevet bredt undersøgt og anvendt i o -
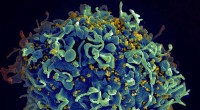 Når HIV-medicin ikke samarbejderHIV inficerer en menneskelig celle. Kredit:NIH Udtrykket synergi har fået et ry som et overbrugt buzzword, men det har en kvantificerbar definition i farmakologi. To lægemidler anses for synergist
Når HIV-medicin ikke samarbejderHIV inficerer en menneskelig celle. Kredit:NIH Udtrykket synergi har fået et ry som et overbrugt buzzword, men det har en kvantificerbar definition i farmakologi. To lægemidler anses for synergist
- $7, 500 føderal skattefradrag for Tesla-købere, der slutter den 31. december
- Sådan arbejder flyselskabets besætninger
- Hvilken plante producerer syrer, der hjælper med kemisk forvitring?
- Nanokrystaller sætter ny aktivitetsrekord for brintproduktion under synlig og nær-infrarød bestrå…
- Undersøgelse afslører årtiers variation af forholdet mellem østasiatisk sommermonsun og El Nino
- Hvordan forklarede Dalton dannelsen af forbindelser?


