Hvad er den molekylære formel af sammensat CH2 med molmasse svarer til 168 gmol?
1. Find den empiriske formelmasse:
* Den empiriske formel er CH2.
* Beregn den molære masse af CH2:12,01 g/mol (c) + 2 * 1,01 g/mol (H) =14,03 g/mol
2. Bestem forholdet mellem den molære masse og den empiriske formelmasse:
* Molmasse af forbindelse / empirisk formelmasse =168 g / mol / 14,03 g / mol =12
3. Multiplicer underskrifterne i den empiriske formel med forholdet:
* CH2 * 12 = C12H24
Derfor er den molekylære formel for forbindelsen C12H24.
 Varme artikler
Varme artikler
-
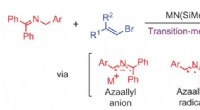 Overgangsmetalfri carbon-carbon-bindingsdannende reaktion:vinylering af azaallylOvergangs-metal-fri vinylering af azaallyl-anioner. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2760 (Phys.org) - Visse funktionelle grupper viser sig ofte i naturlige produkter og biologisk
Overgangsmetalfri carbon-carbon-bindingsdannende reaktion:vinylering af azaallylOvergangs-metal-fri vinylering af azaallyl-anioner. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2760 (Phys.org) - Visse funktionelle grupper viser sig ofte i naturlige produkter og biologisk -
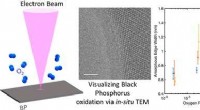 Ingeniører fremmer indsigt i sort fosfor som et materiale til fremtidig fleksibel elektronik med ul…Kredit:ACS Sort fosfor er et krystallinsk materiale, der tiltrækker stigende forskningsinteresse fra halvlederenhedsingeniører, kemikere og materialeforskere til at skabe atomisk tynde film af høj
Ingeniører fremmer indsigt i sort fosfor som et materiale til fremtidig fleksibel elektronik med ul…Kredit:ACS Sort fosfor er et krystallinsk materiale, der tiltrækker stigende forskningsinteresse fra halvlederenhedsingeniører, kemikere og materialeforskere til at skabe atomisk tynde film af høj -
 Fremstilling af kirurgiske instrumenter af medicinsk affaldNye styrbare instrumenter til avanceret laparoskopisk kirurgi, delvist lavet af rustfrit stål og blåt polypropylenbetræk, bliver brugt for første gang på Malta. Kredit:Delft University of Technology
Fremstilling af kirurgiske instrumenter af medicinsk affaldNye styrbare instrumenter til avanceret laparoskopisk kirurgi, delvist lavet af rustfrit stål og blåt polypropylenbetræk, bliver brugt for første gang på Malta. Kredit:Delft University of Technology -
 Harmløse elementer kan erstatte giftigt bly i elektronikHenrik Sønsteby holder en siliciumwafer dækket med en tynd film bestående af natrium, kalium, niobium og oxygen. Farverne er forårsaget af utilsigtede tykkelsesvariationer. Kredit:Bjarne Roesjoe/UiO
Harmløse elementer kan erstatte giftigt bly i elektronikHenrik Sønsteby holder en siliciumwafer dækket med en tynd film bestående af natrium, kalium, niobium og oxygen. Farverne er forårsaget af utilsigtede tykkelsesvariationer. Kredit:Bjarne Roesjoe/UiO
- Hvordan er planeter og stjerner både?
- Hvilke 2 kræfter kan omdanne fossiler til fossile brændstoffer?
- Fysikers undersøgelse viser, at silicium energihøstes
- Hvad er tåregas?
- Placeringen af en stor mystisk kilde til forbudt ozonnedbrydende stof afdækket
- Beyond the Moores Law:Nanocomputing ved hjælp af nanotrådfliser


