Er O3-bindinger polære eller ikke-polære?
* Elektronegativitet: Oxygen har en høj elektronegativitet, hvilket betyder, at det tiltrækker elektroner stærkere end andre atomer.
* bøjet struktur: Ozon har en bøjet molekylær geometri med et centralt iltatom bundet til to andre iltatomer. Denne bøjede struktur betyder, at elektrondensiteten ikke fordeles jævnt.
* ulig deling: Det centrale iltatom er mere elektronegativt end de terminale iltatomer. Dette får elektrondensiteten til at blive trukket mere mod det centrale ilt, hvilket skaber en delvis negativ ladning på den og delvise positive ladninger på de terminale oxygener.
Derfor er O3 -bindingerne polære på grund af den ulige deling af elektroner og molekylets bøjede struktur.
Sidste artikelEr svovl et element eller en forbindelse?
Næste artikelHvor mange mol natriumcarbonat er til stede i 212G?
 Varme artikler
Varme artikler
-
 Forskere udvikler chip, der forbedrer testning og sporing for COVID-19Kredit:University of New Mexico Jeremy Edwards, direktør for Computational Genomics and Technology (CGaT) Laboratory ved University of New Mexico, og hans kolleger hos Centrillion Technologies i P
Forskere udvikler chip, der forbedrer testning og sporing for COVID-19Kredit:University of New Mexico Jeremy Edwards, direktør for Computational Genomics and Technology (CGaT) Laboratory ved University of New Mexico, og hans kolleger hos Centrillion Technologies i P -
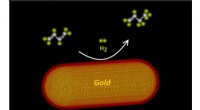 Tværfagligt samarbejde fører til katalysatorer, der er op til 50 gange mere effektiveKemiske reaktioner forekommer på overfladen af bimetalliske nanopartikler. Forskere fandt ud af, at arrangering af de to metaller i et kerneskalledesign gør disse katalysatorer op til 50 gange mere
Tværfagligt samarbejde fører til katalysatorer, der er op til 50 gange mere effektiveKemiske reaktioner forekommer på overfladen af bimetalliske nanopartikler. Forskere fandt ud af, at arrangering af de to metaller i et kerneskalledesign gør disse katalysatorer op til 50 gange mere -
 Forskere afslører reaktive galliumhydrid-arter på galliumoxidoverfladenGrafisk abstrakt. Kredit:Journal of the American Chemical Society (2022). DOI:10.1021/jacs.2c01005 Metalhydrider (M-H), kritiske, men allestedsnærværende mellemprodukter i en bred vifte af katalyti
Forskere afslører reaktive galliumhydrid-arter på galliumoxidoverfladenGrafisk abstrakt. Kredit:Journal of the American Chemical Society (2022). DOI:10.1021/jacs.2c01005 Metalhydrider (M-H), kritiske, men allestedsnærværende mellemprodukter i en bred vifte af katalyti -
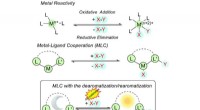 Forståelse af aromaticitet i katalyse for at låse op for nye mulighederFig. 1 Forskellige former for substrataktivering i konventionel og metal-ligand kooperativ katalyse. Kredit: Kemisk kommunikation (2021). DOI:10.1039/D1CC00528F Aromaticitet, et koncept, der norm
Forståelse af aromaticitet i katalyse for at låse op for nye mulighederFig. 1 Forskellige former for substrataktivering i konventionel og metal-ligand kooperativ katalyse. Kredit: Kemisk kommunikation (2021). DOI:10.1039/D1CC00528F Aromaticitet, et koncept, der norm


