Hvad er den ioniske ladning på klor?
Her er hvorfor:
* Elektronkonfiguration: Klor har 17 elektroner. Dens elektronkonfiguration er 2-8-7. Dette betyder, at det har 7 elektroner i sin yderste skal (valenselektroner).
* octet regel: Atomer har en tendens til at vinde eller miste elektroner for at opnå en stabil konfiguration med 8 elektroner i deres yderste skal (Octet -regel).
* At få en elektron: Klor er en elektron væk fra at have en fuld ydre skal. Derfor får det let et elektron for at blive stabilt.
* negativ opladning: Når klor får et elektron, bliver det negativt ladet, betegnet som cl⁻.
Sidste artikelHvilken ladning har klorgas?
Næste artikelHvad er den samlede afgift for klor?
 Varme artikler
Varme artikler
-
 Her kommer solen:en ny ramme for kunstig fotosynteseKredit:RapidEye/iStock Forskere har længe forsøgt at efterligne den proces, hvorved planter fremstiller deres eget brændstof ved hjælp af sollys, carbondioxid, og vand gennem kunstige fotosyntesea
Her kommer solen:en ny ramme for kunstig fotosynteseKredit:RapidEye/iStock Forskere har længe forsøgt at efterligne den proces, hvorved planter fremstiller deres eget brændstof ved hjælp af sollys, carbondioxid, og vand gennem kunstige fotosyntesea -
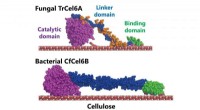 Bakteriel cellulosenedbrydningssystem kunne sætte skub i produktionen af biobrændstofferStrukturelle modeller af svampe- og bakteriecellobiohydrolaser (TrCel6A, CfCel6B) Kredit:NINS/IMS Bestræbelser på at finde måder at nedbryde cellulose - de hårde ting, der udgør plantecellevægge -
Bakteriel cellulosenedbrydningssystem kunne sætte skub i produktionen af biobrændstofferStrukturelle modeller af svampe- og bakteriecellobiohydrolaser (TrCel6A, CfCel6B) Kredit:NINS/IMS Bestræbelser på at finde måder at nedbryde cellulose - de hårde ting, der udgør plantecellevægge - -
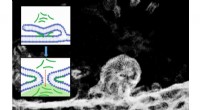 Hvordan trænger peptider ind i celler? To sider af samme møntElektronmikroskopibillede af en todelt cellemembran og det tilsvarende molekylære skema for processen. Kredit:@ IOCB Prag Den simple transport af lægemidler direkte ind i cellerne er et af de prim
Hvordan trænger peptider ind i celler? To sider af samme møntElektronmikroskopibillede af en todelt cellemembran og det tilsvarende molekylære skema for processen. Kredit:@ IOCB Prag Den simple transport af lægemidler direkte ind i cellerne er et af de prim -
 Paradigmeskiftende teori fremhæver vigtigheden af substratfleksibilitet i enzymatiske reaktionerMikroskopisk billede af planteceller af almindelig æblemos (Bartramia pomiformis), med cellevægge, der indeholder xylan. Kredit:Leiden Universitet Leidenske kemikere har foreslået en ny model for
Paradigmeskiftende teori fremhæver vigtigheden af substratfleksibilitet i enzymatiske reaktionerMikroskopisk billede af planteceller af almindelig æblemos (Bartramia pomiformis), med cellevægge, der indeholder xylan. Kredit:Leiden Universitet Leidenske kemikere har foreslået en ny model for
- Stiger energien eller falder energi, når gas bliver en væske?
- Hele huse fejet væk af Irma på Bransons ø
- Hvilke egenskaber har solen til fælles med andre stjerner?
- Hvordan en 'dirigent' giver mening med kaos i tidlige museembryoner
- Billede:Fra jorden, månen og videre
- Udforsk kemien bag kærlighed denne Valentinsdag


