Kobber II sulfat og blynitrat?
Her er hvad der sker:
* reaktanterne:
* Kobber (II) sulfat (cuso₄) er et blåt krystallinsk fast stof, der opløses i vand til dannelse af blå ioner.
* Bly (ii) nitrat (Pb (no₃) ₂) er et hvidt krystallinsk fast stof, der også opløses i vand for at danne farveløse ioner.
* reaktionen: Når du blander opløsninger af kobber (II) sulfat og bly (ii) nitrat, skifter ionerne partnere. Dette resulterer i dannelsen af to nye produkter:
* bly (ii) sulfat (PBSO₄): Dette er et hvidt, uopløseligt fast stof, der udfældes ud af opløsningen som et fast stof.
* kobber (II) nitrat (Cu (no₃) ₂): Dette er en blå løsning, der forbliver opløst.
* den afbalancerede kemiske ligning:
Cuso₄ (aq) + pb (no₃) ₂ (aq) → pbso₄ (s) + cu (no₃) ₂ (aq)
Nøgleobservationer:
* Dannelse af et bundfald: Det mest åbenlyse tegn på reaktionen er dannelsen af et hvidt fast stof (bly (II) sulfat), der sætter sig til bunden af beholderen.
* farveændring: Opløsningen vil ændre farve fra blå (kobber (II) sulfat) til en lettere blå eller farveløs (kobber (II) nitrat).
Ansøgninger:
Denne reaktion har flere praktiske anvendelser:
* Behandling af blyforgiftning: Blysulfat er mindre opløselig end blynitrat, hvilket gør det mindre let absorberet i kroppen. Denne reaktion bruges undertiden til at hjælpe med at fjerne bly fra kroppen i tilfælde af blyforgiftning.
* forberedelse af bly (ii) sulfat: Bly (ii) sulfat bruges til produktion af batterier, pigmenter og andre materialer.
Fortæl mig, hvis du har andre spørgsmål om denne reaktion!
Sidste artikelHvilket atom har yderligere to protoner og elektroner end brom?
Næste artikelHvordan ser brintgas ud?
 Varme artikler
Varme artikler
-
 Kontrol af kunstige cilia med magnetfelter og lysFotografi af en række magnetiske cilia foldet og holdt i spidsen af pincet. Kredit:Jessica A.-C. Liu Forskere fra North Carolina State University og Elon University har lavet kunstige cilia, ell
Kontrol af kunstige cilia med magnetfelter og lysFotografi af en række magnetiske cilia foldet og holdt i spidsen af pincet. Kredit:Jessica A.-C. Liu Forskere fra North Carolina State University og Elon University har lavet kunstige cilia, ell -
 Bærbar enhed belyser vejen til bedre opdagelse af fødevarebårne sygdommeForskere fra Purdue University skabte en bærbar enhed, der arbejder med smartphones og bærbare computere til at foretage test på stedet for E. coli i madprøver. Kredit:Euiwon Bae/Purdue University
Bærbar enhed belyser vejen til bedre opdagelse af fødevarebårne sygdommeForskere fra Purdue University skabte en bærbar enhed, der arbejder med smartphones og bærbare computere til at foretage test på stedet for E. coli i madprøver. Kredit:Euiwon Bae/Purdue University -
 At skabe nul-energihuse, giftfri glitter og fossilfri lim med træNulenergihus Luukku. Kredit:Montse Zamorano At bygge klogt med træ er en effektiv måde at bekæmpe klimaændringer på. Det er muligt at bygge næsten alt med træ, hvis vi udvikler vores ekspertise og
At skabe nul-energihuse, giftfri glitter og fossilfri lim med træNulenergihus Luukku. Kredit:Montse Zamorano At bygge klogt med træ er en effektiv måde at bekæmpe klimaændringer på. Det er muligt at bygge næsten alt med træ, hvis vi udvikler vores ekspertise og -
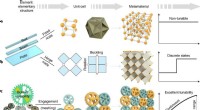 Gear-baserede mekaniske metamaterialer giver mulighed for oprettelse af konfigurerbare arkDesignkoncepter af mekaniske metamaterialer. a,b, klassisk paradigme:ikke-afstembart metamateriale (a) og typisk rekonfigurerbart metamateriale (b). c, Gear-baserede metamaterialer. Kredit:Nature Mate
Gear-baserede mekaniske metamaterialer giver mulighed for oprettelse af konfigurerbare arkDesignkoncepter af mekaniske metamaterialer. a,b, klassisk paradigme:ikke-afstembart metamateriale (a) og typisk rekonfigurerbart metamateriale (b). c, Gear-baserede metamaterialer. Kredit:Nature Mate
- Udskrivning af trådløst genopladelige solid-state superkapacitorer til bløde, smarte kontaktlinse…
- Nye australske love kunne se, at ledere på sociale medier blev fængslet over terrorbilleder
- $100 millioner spørgsmål:Hvor er bredbånd i USA?
- Ny undersøgelse fremhæver overdrevne fysiske forskelle mellem mandlige og kvindelige superhelte
- Oplysninger om Exide GC135 Batteri
- Flersprogede elever har forbedret deres akademiske præstationer siden 2003


