Hvor mange ensomme par elektroner er persent i en molekyle ammoniak?
Her er hvorfor:
* nitrogen's valenselektroner: Nitrogen har 5 valenselektroner.
* bindinger med brint: I ammoniak danner nitrogen tre enkeltbindinger med tre hydrogenatomer. Hver binding involverer deling af et elektron fra nitrogen og en fra brint.
* resterende elektroner: Dette efterlader to af nitrogens valenselektroner ubundet. Disse to elektroner danner et ensomt par.
Du kan visualisere dette med en Lewis -struktur:
H
|
H - N - H
|
H
De to prikker på nitrogenet repræsenterer det ensomme par.
 Varme artikler
Varme artikler
-
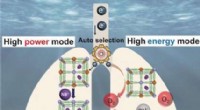 Energi fra havvand:Powergeneratoren skifter autonomt mellem to funktionelle tilstandeKredit:Wiley Undervandsfartøjer, dykkerrobotter, og detektorer kræver deres egen energiforsyning for at fungere i lange perioder uafhængigt af skibe. En ny, billigt system til direkte elektrokemis
Energi fra havvand:Powergeneratoren skifter autonomt mellem to funktionelle tilstandeKredit:Wiley Undervandsfartøjer, dykkerrobotter, og detektorer kræver deres egen energiforsyning for at fungere i lange perioder uafhængigt af skibe. En ny, billigt system til direkte elektrokemis -
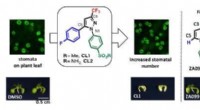 Flere mund kan fodres ved at øge antallet af plantens porerForbindelser, der øger antallet af stomata på planter. Kredit:Nagoya University Miljøundersøgelser har vist, at 40% af det atmosfæriske kuldioxid (CO2) passerer hvert år gennem plantemateriale. De
Flere mund kan fodres ved at øge antallet af plantens porerForbindelser, der øger antallet af stomata på planter. Kredit:Nagoya University Miljøundersøgelser har vist, at 40% af det atmosfæriske kuldioxid (CO2) passerer hvert år gennem plantemateriale. De -
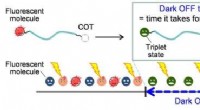 Når FRETING over cancerbiomarkører ikke virker, fokusere på at blinke i stedet forSkematisk repræsentation af fluorescensblink styret af tripletdannelse og triplet-triplet energioverførsel. Kredit:Osaka University Fluorescensspektroskopi er uundværlig i biomedicinsk diagnostik.
Når FRETING over cancerbiomarkører ikke virker, fokusere på at blinke i stedet forSkematisk repræsentation af fluorescensblink styret af tripletdannelse og triplet-triplet energioverførsel. Kredit:Osaka University Fluorescensspektroskopi er uundværlig i biomedicinsk diagnostik. -
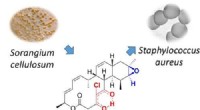 Antimikrobielt naturprodukt, der er aktivt mod både MRSA og malariaforårsagende parasitAnaloger af det naturlige produkt chlorotonil blev opnået ved semisyntese gennem regio- og stereoselektiv epoxidation og efterfølgende ringåbning. Derivaterne bibeholdt aktivitet mod multiresistente g
Antimikrobielt naturprodukt, der er aktivt mod både MRSA og malariaforårsagende parasitAnaloger af det naturlige produkt chlorotonil blev opnået ved semisyntese gennem regio- og stereoselektiv epoxidation og efterfølgende ringåbning. Derivaterne bibeholdt aktivitet mod multiresistente g
- Hvad placerede Allesandro Volta mellem lag af metal?
- Hvad er talteori?
- Hvad er kvalitativt forhold mellem kraft og potentiel energi?
- Nintendo udgiver remasterede Mario-klassikere til Switch i 2020
- Hvad er de hvide ting, der falder fra himlen?
- Spolede nanotråde kan indeholde nøglen til strækbar elektronik


