Er der en kemisk reaktion mellem Srcl2 og Cocl2?
Her er hvorfor:
* begge er opløselige salte: SRCL₂ og COCL₂ er begge opløselige ioniske forbindelser. Når de opløses i vand, adskiller de sig i deres respektive ioner:SR²⁺, Cl⁻, CO²⁺ og Cl⁻.
* Ingen drivkraft til reaktion: Der er ingen stærk drivkraft for, at der forekommer en reaktion mellem disse ioner.
* Ingen bundfaldsdannelse: De potentielle produkter, SRCL₂ og COCL₂, er begge opløselige salte, så der ville ikke dannes noget bundfald.
* Ingen gasudvikling: Ingen gasser genereres.
* Ingen signifikant varmeændring: Reaktionen er sandsynligvis ikke meget eksoterm eller endotermisk.
Kortfattet: Ionerne i opløsning vil simpelthen sameksistere som separate enheder. Der er ingen overbevisende grund til, at de reagerer og danner nye forbindelser.
 Varme artikler
Varme artikler
-
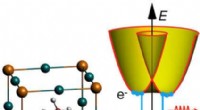 Lyser på rekombinationsmekanismer i solcellematerialerStærk spin-orbit-kobling i halogenidperovskitter inducerer spaltning af båndkanterne, hvilket kan påvirke rekombinationshastigheden. Kredit:X. Zhang og J.-X. Shen Hybride perovskiter er spektakulæ
Lyser på rekombinationsmekanismer i solcellematerialerStærk spin-orbit-kobling i halogenidperovskitter inducerer spaltning af båndkanterne, hvilket kan påvirke rekombinationshastigheden. Kredit:X. Zhang og J.-X. Shen Hybride perovskiter er spektakulæ -
 Konstrueret gær kunne udvide biobrændstoffers rækkeviddeKredit:CC0 Public Domain At øge produktionen af biobrændstoffer som ethanol kan være et vigtigt skridt i retning af at reducere det globale forbrug af fossile brændstoffer. Imidlertid, ethanolpr
Konstrueret gær kunne udvide biobrændstoffers rækkeviddeKredit:CC0 Public Domain At øge produktionen af biobrændstoffer som ethanol kan være et vigtigt skridt i retning af at reducere det globale forbrug af fossile brændstoffer. Imidlertid, ethanolpr -
 Ny PET-lignende plast fremstillet direkte fra affaldsbiomasseEt 3D-printet blad lavet med den nye bioplast. Kredit:Alain Herzog (EPFL) Det bliver mere og mere indlysende, at det at flytte væk fra fossile brændstoffer og undgå akkumulering af plastik i miljøe
Ny PET-lignende plast fremstillet direkte fra affaldsbiomasseEt 3D-printet blad lavet med den nye bioplast. Kredit:Alain Herzog (EPFL) Det bliver mere og mere indlysende, at det at flytte væk fra fossile brændstoffer og undgå akkumulering af plastik i miljøe -
 Forskere udvikler en ny tilgang til at forudsige, hvordan væsker fryserKredit:Pixabay/CC0 Public Domain Forskere fra Queen Mary University of London har udviklet en ny beregningsmetode til bedre at forstå frysning i forskellige typer væsker. Processen med at fryse,
Forskere udvikler en ny tilgang til at forudsige, hvordan væsker fryserKredit:Pixabay/CC0 Public Domain Forskere fra Queen Mary University of London har udviklet en ny beregningsmetode til bedre at forstå frysning i forskellige typer væsker. Processen med at fryse,
- Tilfældet med Brasilien:Hvordan politiske beslutningstagere kan reducere undgåelige dødsfald på …
- Hvilke planeter har vi besøgt?
- Kunne vi installere kæmpe spejle i rummet mellem jord og sol for at aflede sollys?
- Hvordan kunne du bevise, at magnesium er et mere reaktivt metal end zink eller jern?
- Hvorfor kræver nogle materialer ikke skæringsvæsker, der skal bruges?
- Verizon:Ingen internethastighedsbegrænsninger for første respondenter


