Hvad er den afbalancerede reaktionsligning mellem natriumthiosulfat og molekylær jod?
2 na₂s₂o₃ + i₂ → na₂s₄o₆ + 2 nai
Her er sammenbruddet:
* reaktanter:
* Natriumthiosulfat (Na₂s₂o₃) - En hvid krystallinsk fast stof
* Molekylær jod (i₂) - Et lilla -sort fast stof
* Produkter:
* Natriumtetrathionat (na₂s₄o₆) - En farveløs løsning
* Natriumiodid (NAI) - En farveløs løsning
Forklaring:
Reaktionen involverer en redox -proces, hvor jod (I₂) reduceres, og thiosulfat (s₂o₃²⁻) oxideres.
* Oxidation: To thiosulfationer (S₂O₃²⁻) oxideres til tetrathionat (S₄O₆²⁻) ved at miste elektroner.
* reduktion: Et jodmolekyle (I₂) reduceres til to iodidioner (I⁻) ved at vinde elektroner.
Denne reaktion bruges ofte i analytisk kemi til at bestemme koncentrationen af jodopløsninger (iodometri). Forsvinden af den brune jodfarve bruges til at indikere slutpunktet for reaktionen.
 Varme artikler
Varme artikler
-
 Forskere dechifrerer strukturen af lovende metalorganiske rammerForskere ved MIT og andre institutioner har fundet en måde at stabilisere væksten af krystaller af flere slags metalorganiske rammer, eller MOFer. Dette billede viser to scanning elektronmikroskopi
Forskere dechifrerer strukturen af lovende metalorganiske rammerForskere ved MIT og andre institutioner har fundet en måde at stabilisere væksten af krystaller af flere slags metalorganiske rammer, eller MOFer. Dette billede viser to scanning elektronmikroskopi -
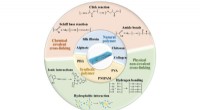 Hydrogel fremmer sårheling bedre end traditionelle bandager, gazebindTværbindingsmekanismer og råmaterialer til forskellige hydrogel sårbandager. Kredit:Zheng Pan, Huijun Ye, og Decheng Wu Den udbredte brug af højhastigheds- og højenergivåben i moderne krigsførelse
Hydrogel fremmer sårheling bedre end traditionelle bandager, gazebindTværbindingsmekanismer og råmaterialer til forskellige hydrogel sårbandager. Kredit:Zheng Pan, Huijun Ye, og Decheng Wu Den udbredte brug af højhastigheds- og højenergivåben i moderne krigsførelse -
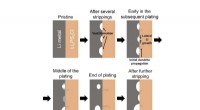 Fremme i forståelsen af all-solid-state batterierSkematisk af Li-metal/Li6PS5Cl-grænsefladen cyklet ved en samlet strømtæthed over CCS. Kredit: Naturmaterialer (2019) All-solid-state batterier, et batteridesign bestående af alle solide komponen
Fremme i forståelsen af all-solid-state batterierSkematisk af Li-metal/Li6PS5Cl-grænsefladen cyklet ved en samlet strømtæthed over CCS. Kredit: Naturmaterialer (2019) All-solid-state batterier, et batteridesign bestående af alle solide komponen -
 At bryde reglerne:Tunge kemiske grundstoffer ændrer teorien om kvantemekanikThomas Albrecht-Schmitt er Gregory R. Choppin professor i kemi ved Florida State University. Kredit:Bill Lax/FSU Photography Services En række komplicerede eksperimenter, der involverer et af de m
At bryde reglerne:Tunge kemiske grundstoffer ændrer teorien om kvantemekanikThomas Albrecht-Schmitt er Gregory R. Choppin professor i kemi ved Florida State University. Kredit:Bill Lax/FSU Photography Services En række komplicerede eksperimenter, der involverer et af de m
- Hvordan identificerer atomnummeret atomer i et bestemt element?
- Australien fyrer langt fra slut, men regn bringer lindring
- Hvor meget stiger temperaturen i det næste århundrede?
- Hvad er antallet af rotationer på Jupiter?
- Sådan fungerer hydrauliske kraner
- Forklar virkningerne af tryk og temperatur på skifer?


