Hvad er den empiriske formel for jernchlorid, hvis det indeholder 55,85 gram og 106,5 klor?
1. Konverter gram til mol
* jern (Fe): 55,85 g Fe / 55,845 g / mol Fe =1.000 mol Fe
* klor (Cl): 106,5 g Cl / 35,45 g / mol Cl =3.000 mol Cl
2. Find molforholdet
* Opdel antallet af mol af hvert element med det mindste antal mol (hvilket er 1.000 mol i dette tilfælde):
* Fe:1.000 mol / 1.000 mol =1
* Cl:3.000 mol / 1.000 mol =3
3. Skriv den empiriske formel
* Molforholdet fortæller os, at den empiriske formel er fecl₃ .
Derfor er den empiriske formel for jernchlorid med disse proportioner fecl₃.
 Varme artikler
Varme artikler
-
 Kortlægning af solcellernes energiske landskabKredit:CC0 Public Domain En ny spektroskopisk metode gør det nu muligt at måle og visualisere det energiske landskab inde i solceller baseret på organiske materialer. Det blev udviklet af et forsk
Kortlægning af solcellernes energiske landskabKredit:CC0 Public Domain En ny spektroskopisk metode gør det nu muligt at måle og visualisere det energiske landskab inde i solceller baseret på organiske materialer. Det blev udviklet af et forsk -
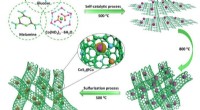 S, N co-doteret carbon nanorør-indkapslet CoS2@CoSkematisk illustration og fysisk karakterisering af S, N co-dopede kulstof nanorør indkapslede kerne-skal (CoS2@Co) nanopartikler. Kredit:©Science China Press Elektrokemisk vandopdeling er en guns
S, N co-doteret carbon nanorør-indkapslet CoS2@CoSkematisk illustration og fysisk karakterisering af S, N co-dopede kulstof nanorør indkapslede kerne-skal (CoS2@Co) nanopartikler. Kredit:©Science China Press Elektrokemisk vandopdeling er en guns -
 Åbner den sorte boks af heterogen katalyseKredit:Institut for Kemisk Forskning i Catalonien Forskere fra ICIQs López-gruppe præsenterer en ny metode, der giver mulighed for rationelt design af heterogene katalysatorer. Efter anvendelse af
Åbner den sorte boks af heterogen katalyseKredit:Institut for Kemisk Forskning i Catalonien Forskere fra ICIQs López-gruppe præsenterer en ny metode, der giver mulighed for rationelt design af heterogene katalysatorer. Efter anvendelse af -
 En intelligent, formformende, selvhelbredende materiale til integreret kunstig muskel og nervevævForskere udvikler et formformende materiale med en hidtil uset multifunktionalitet til blød robotik og bærbar elektronik. Kredit:Soft Machines Lab, Carnegie Mellon University Fremskridt inden for
En intelligent, formformende, selvhelbredende materiale til integreret kunstig muskel og nervevævForskere udvikler et formformende materiale med en hidtil uset multifunktionalitet til blød robotik og bærbar elektronik. Kredit:Soft Machines Lab, Carnegie Mellon University Fremskridt inden for
- Hvordan kredserer GPS -satellitsystemer?
- Ny metode afslører mysteriet med langsomme elektroner
- Mulige fejl i loveksperiment?
- Hvad mener forskere kan være resterne af en planet, der engang eksisterede i vores solsystem?
- Hvad er en elektrisk kondensator?
- Hvilken blev opfundet første pære mikrobølgeovn eller telefon?


