Hvor mange gram RM NH3 kan produceres fra 2,90 mol N2?
1. Afbalanceret kemisk ligning:
Den afbalancerede kemiske ligning til reaktion af nitrogengas (N₂) med brintgas (H₂) til at producere ammoniak (NH₃) er:
N₂ + 3H₂ → 2NH₃
2. Molforhold:
Fra den afbalancerede ligning ser vi, at 1 mol N₂ producerer 2 mol NH₃.
3. Beregning:
* Vi har 2,90 mol N₂.
* Ved hjælp af molforholdet kan vi finde molen af NH₃ produceret:2,90 mol N₂ * (2 mol NH₃ / 1 mol N₂) =5,80 mol NH₃
4. Konverter mol til gram:
* Den molære masse af NH₃ er 17,03 g/mol (14,01 g/mol for N + 3 * 1,01 g/mol for H)
* Multiplicer molen af NH₃ med dens molære masse for at få massen i gram:5,80 mol NH₃ * 17,03 g/mol = 98,7 g NH₃
Derfor kan 98,7 gram NH₃ produceres fra 2,90 mol n₂.
Sidste artikelHvilke metaller er ikke magnetiske?
Næste artikelHvilken type binding holder atomer sammen i et calciumchloridmolekyle?
 Varme artikler
Varme artikler
-
 Den grundlæggende kemi bag elektrokatalytisk vandspaltningOxygen evolution reaktion. Kredit:Matthias Frei, ETH Zürich Overgang til en bæredygtig energiøkonomi kræver elektrokatalytiske metoder til at konvertere elektrisk energi til kemisk energi og råsto
Den grundlæggende kemi bag elektrokatalytisk vandspaltningOxygen evolution reaktion. Kredit:Matthias Frei, ETH Zürich Overgang til en bæredygtig energiøkonomi kræver elektrokatalytiske metoder til at konvertere elektrisk energi til kemisk energi og råsto -
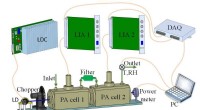 Ny sensor til måling af atmosfæriske aerosoler og nitrogendioxid samtidigtEksperimentel opsætning af D-PAS. Kredit:LIU Kun For nylig, Prof. 2 ) samtidigt. Atmosfæriske aerosoler og NO 2 betragtes som de vigtigste forurenende stoffer i luften, mens online måling af
Ny sensor til måling af atmosfæriske aerosoler og nitrogendioxid samtidigtEksperimentel opsætning af D-PAS. Kredit:LIU Kun For nylig, Prof. 2 ) samtidigt. Atmosfæriske aerosoler og NO 2 betragtes som de vigtigste forurenende stoffer i luften, mens online måling af -
 Forskere producerer smart stof til at neutralisere nervegasTeresa Bandosz. Kredit:City College i New York Fra laboratoriet i City College i New York kemiingeniør og Fulbright Scholar Teresa J. Bandosz kommer en banebrydende udvikling med potentiale til at
Forskere producerer smart stof til at neutralisere nervegasTeresa Bandosz. Kredit:City College i New York Fra laboratoriet i City College i New York kemiingeniør og Fulbright Scholar Teresa J. Bandosz kommer en banebrydende udvikling med potentiale til at -
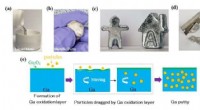 Spartellignende kompositter af galliummetal med potentiale til anvendelse i virkeligheden(a) Flydende gallium hældes i en beholder. (b) Galliumkitt støbes til en kugle. (c) Forskellige figurer fremstillet af galliumspartel. (d) Galliumspartel skæres af et blad. (e) Mekanismen for dannelse
Spartellignende kompositter af galliummetal med potentiale til anvendelse i virkeligheden(a) Flydende gallium hældes i en beholder. (b) Galliumkitt støbes til en kugle. (c) Forskellige figurer fremstillet af galliumspartel. (d) Galliumspartel skæres af et blad. (e) Mekanismen for dannelse


