Hvor mange chloridioner er i 1,50 mol aluminiumchlorid?
1. Forstå formlen
Aluminiumchlorid har den kemiske formel alcl₃. Dette betyder, at hver formelenhed indeholder en aluminiumion (al³⁺) og tre chloridioner (CL⁻).
2. Brug molforholdet
* For hver 1 mol alcl₃ er der 3 mol cl⁻ioner.
3. Beregn antallet af chloridioner
* Start med molen af alcl₃:1,50 mol alcl₃
* Multiplicer med molforholdet:(1,50 mol alcl₃) * (3 mol cl⁻ / 1 mol alcl₃) =4,50 mol cl⁻
4. Konverter mol til ioner
* Brug Avogadros nummer (6,022 x 10²³ ioner/mol) til at omdanne mol chloridioner til antallet af ioner:
(4,50 mol cl⁻) * (6,022 x 10²³ ioner/mol) = 2,71 x 10²⁴ chloridioner
Derfor er der 2,71 x 10²⁴chloridioner i 1,50 mol aluminiumchlorid.
Sidste artikelReaktion af bariumchlorid med sølvnitrat?
Næste artikelHvilke metaller er ikke magnetiske?
 Varme artikler
Varme artikler
-
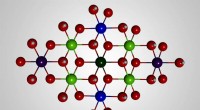 Forskning afslører mekanismen bag en vandspaltningskatalysatorBall-and-stick model af molekylstrukturen af sol-brændstof-katalysatoren udviklet hos Caltech. Blå repræsenterer jernatomer; grøn er nikkel; rød er oxygen; hvid er brint. Kredit:Caltech Caltech-
Forskning afslører mekanismen bag en vandspaltningskatalysatorBall-and-stick model af molekylstrukturen af sol-brændstof-katalysatoren udviklet hos Caltech. Blå repræsenterer jernatomer; grøn er nikkel; rød er oxygen; hvid er brint. Kredit:Caltech Caltech- -
 Salt tager et hurtigt skridt, før det falder ud af vandetI et fund med konsekvenser for emner, herunder klimamodeller og lægemiddelproduktion, beregningsmæssig forskning fra Princeton University har beskrevet et yderligere trin i udfældningen af saltkryst
Salt tager et hurtigt skridt, før det falder ud af vandetI et fund med konsekvenser for emner, herunder klimamodeller og lægemiddelproduktion, beregningsmæssig forskning fra Princeton University har beskrevet et yderligere trin i udfældningen af saltkryst -
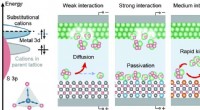 Vulkanformet trend muliggør rationelt design af polysulfidkatalysatorer i lithium-svovlbatterierSkematisk diagram af designprincipper for højeffektive lithium-svovl-katalysatorer. Kredit:Shen Zihan Et fælles forskerhold ledet af prof. Zhang Huigang fra Institute of Process Engineering (IPE) v
Vulkanformet trend muliggør rationelt design af polysulfidkatalysatorer i lithium-svovlbatterierSkematisk diagram af designprincipper for højeffektive lithium-svovl-katalysatorer. Kredit:Shen Zihan Et fælles forskerhold ledet af prof. Zhang Huigang fra Institute of Process Engineering (IPE) v -
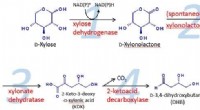 Metabolisk ingeniørmetode lykkes med at producere 1, 2, 4-butantetriol bæredygtigt fra biomasseFigur 1:Diagram over reaktionsprocessen. Kredit:Kobe University En mere miljøvenlig og bæredygtig metode til fremstilling af det nyttige kemikalie 1, 2, 4-butantetriol er blevet opdaget. Kobe -uni
Metabolisk ingeniørmetode lykkes med at producere 1, 2, 4-butantetriol bæredygtigt fra biomasseFigur 1:Diagram over reaktionsprocessen. Kredit:Kobe University En mere miljøvenlig og bæredygtig metode til fremstilling af det nyttige kemikalie 1, 2, 4-butantetriol er blevet opdaget. Kobe -uni
- Belysning af strukturelle egenskaber i Li-ion-batterier, der leverer ultrahurtig opladning
- Hvad er enheden med en frekvens?
- Hvad er det koldeste sted på jorden?
- Højteknologiske laserscanninger afslører skjult militær travers på Alcatraz Island
- Hvilke bølger overfører termisk energi?
- 6 Oplever store eller små populationer mere genetisk drift?


