Hvilket stof har højere smeltepunkt siliciumdioxid eller methanol?
* siliciumdioxid (SiO2) er et netværk kovalent fast. Dette betyder, at det danner en kæmpe, tredimensionel struktur, hvor siliciumatomer er bundet til iltatomer i et kontinuerligt netværk. Disse stærke kovalente bindinger kræver en masse energi til at bryde, hvilket resulterer i et meget højt smeltepunkt (ca. 1713 ° C).
* methanol (CH3OH) er en molekylær forbindelse, der holdes sammen af relativt svage intermolekylære kræfter (hydrogenbinding). Disse kræfter er meget svagere end de kovalente bindinger i SiO2. Derfor har methanol et meget lavere smeltepunkt (-97,6 ° C).
Kortfattet:
* siliciumdioxid (SiO2) - højt smeltepunkt på grund af stærke kovalente bindinger.
* Methanol (CH3OH) - Lavt smeltepunkt på grund af svage intermolekylære kræfter.
Sidste artikelHvorfor har klor eller silicium et højere smeltepunkt?
Næste artikelEr smeltende kobber en eksoterme proces?
 Varme artikler
Varme artikler
-
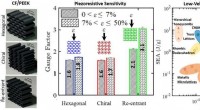 Letvægts, slagfaste bikagestrukturer kan fornemme, når de er blevet beskadigetGrafisk abstrakt. Kredit: Materialer og design (2021). DOI:10.1016/j.matdes.2021.109863 En ny form for letvægts, slagfaste plastbaserede honningkage-strukturer, der kan mærke, hvornår de er bleve
Letvægts, slagfaste bikagestrukturer kan fornemme, når de er blevet beskadigetGrafisk abstrakt. Kredit: Materialer og design (2021). DOI:10.1016/j.matdes.2021.109863 En ny form for letvægts, slagfaste plastbaserede honningkage-strukturer, der kan mærke, hvornår de er bleve -
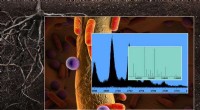 Optrævling af den molekylære kompleksitet af cellulære maskiner og miljøprocesser21-Tesla Fourier transformation ion cyclotron resonans massespektrometer (data vist til højre) vil drive den fremtidige retning af miljø, biologiske, atmosfærisk, og energiforskning. Kredit:Pacific No
Optrævling af den molekylære kompleksitet af cellulære maskiner og miljøprocesser21-Tesla Fourier transformation ion cyclotron resonans massespektrometer (data vist til højre) vil drive den fremtidige retning af miljø, biologiske, atmosfærisk, og energiforskning. Kredit:Pacific No -
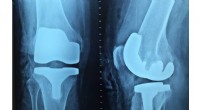 Forbedret menneskelig kropsreaktion på implantaterKredit:pixabay UPM-forskere har udviklet en ny overfladebehandling for at reducere afstødning af metalliske biomaterialeimplantater. Dette vil forlænge protesens levetid og dermed øge livskvalitet
Forbedret menneskelig kropsreaktion på implantaterKredit:pixabay UPM-forskere har udviklet en ny overfladebehandling for at reducere afstødning af metalliske biomaterialeimplantater. Dette vil forlænge protesens levetid og dermed øge livskvalitet -
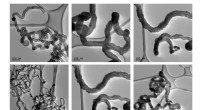 Fra genbrug til upcycling:En smartere måde at håndtere plast påEksempler på carbon nanorør produceret med den nye tilgang, ved forskellige forstørrelser. Kredit:RMIT University Globalt genbruges kun omkring 20% af affaldsplast. At øge dette tal er stadig en
Fra genbrug til upcycling:En smartere måde at håndtere plast påEksempler på carbon nanorør produceret med den nye tilgang, ved forskellige forstørrelser. Kredit:RMIT University Globalt genbruges kun omkring 20% af affaldsplast. At øge dette tal er stadig en


