Hvilken reaktion sker mellem vandigt klor- og natriumbromidopløsning?
Her er den afbalancerede kemiske ligning:
cl₂ (aq) + 2nabr (aq) → 2naCl (aq) + br₂ (aq)
Forklaring:
* klor (cl₂) er mere reaktiv end brom (br₂) . Dette betyder, at klor har en stærkere tendens til at vinde elektroner og danne negative ioner.
* Når chlor tilsættes til en opløsning af natriumbromid, reagerer chloratomerne med bromidionerne (BR-) for at danne brommolekyler (BR₂) og chloridioner (CL-).
* Natriumionerne (Na+) forbliver i opløsning og danner natriumchlorid (NaCl).
Observation:
Reaktionen resulterer i dannelsen af en brunlig-rød opløsning På grund af tilstedeværelsen af brom. Løsningen kan også have en lidt skarp lugtegenskab for brom.
Vigtig note:
Denne reaktion er et klassisk eksempel på en halogenfortrængningsreaktion . Halogener (gruppe 17 -elementer) er meget reaktive og kan fortrænge hinanden fra deres forbindelser efter tendensen med reaktivitet:
* fluor (f₂)> chlor (cl₂)> brom (br₂)> jod (i₂)> astatine (at)
Dette betyder, at fluor kan fortrænge klor, klor kan fortrænge brom osv.
Sidste artikelHvad sker der, når natriumchlorid og bromvand blandes?
Næste artikelHvad er symbolligningen for natrium og brom?
 Varme artikler
Varme artikler
-
 Ved hjælp af to CRISPR -enzymer, en COVID -diagnose på kun 20 minutterReaktionerne involveret i FIND-IT-assayet for at påvise infektion med SARS-CoV-2-virussen. Når Cas13 -enzymet (nederst til venstre) binder sig til sit mål -RNA, det klipper et molekyle (orange og lyse
Ved hjælp af to CRISPR -enzymer, en COVID -diagnose på kun 20 minutterReaktionerne involveret i FIND-IT-assayet for at påvise infektion med SARS-CoV-2-virussen. Når Cas13 -enzymet (nederst til venstre) binder sig til sit mål -RNA, det klipper et molekyle (orange og lyse -
 Kræft målrettet med genanvendelig brændenældebehandlingRepræsentation af den organiske osmiumforbindelse, som udløses ved hjælp af en ikke-toksisk dosis natriumformiat, et naturligt produkt, der findes i mange organismer, herunder brændenælder og myrer. K
Kræft målrettet med genanvendelig brændenældebehandlingRepræsentation af den organiske osmiumforbindelse, som udløses ved hjælp af en ikke-toksisk dosis natriumformiat, et naturligt produkt, der findes i mange organismer, herunder brændenælder og myrer. K -
 Den søde smag af succes for en understøttet nikkel -legeringskatalysator af nikkelphosphidKatalytisk hydrogenering af maltose til maltitol. Kredit:Osaka University Katalysatorer er kernen i en grønnere og mere bæredygtig fremtid for kemisk produktion. Imidlertid, mange af de katalysato
Den søde smag af succes for en understøttet nikkel -legeringskatalysator af nikkelphosphidKatalytisk hydrogenering af maltose til maltitol. Kredit:Osaka University Katalysatorer er kernen i en grønnere og mere bæredygtig fremtid for kemisk produktion. Imidlertid, mange af de katalysato -
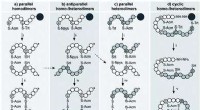 Bioinspirerede strategier til udvikling af nye lægemidlerFig. 1 Syntetiske strategier mod parallelle, antiparallelle og cykliske to-disulfidbindingshomo- og heterodimerer af VP/OT. Anvendte ortogonale beskyttelsesgrupper:Acm, acetamidomethyl; Npys, 3-nitro
Bioinspirerede strategier til udvikling af nye lægemidlerFig. 1 Syntetiske strategier mod parallelle, antiparallelle og cykliske to-disulfidbindingshomo- og heterodimerer af VP/OT. Anvendte ortogonale beskyttelsesgrupper:Acm, acetamidomethyl; Npys, 3-nitro
- Science Fair Project for at teste, om synet påvirker Taste
- Hvad er den fase, der opstår efter en hovedsekvensstjerne?
- Hvorfor ændres arrangementet af konstellationer gennem sæsoner?
- Hvad er usædvanligt ved peridotit og dunite?
- Hvad er fysik, og hvorfor er det navngivet som fysik?
- Forskere udvikler en statistisk løsning på arkæologiske dateringsproblem


