Er ammoniumion et reducerende eller oxidationsmiddel?
* Oxidationstilstand af nitrogen: I ammoniumion har nitrogen en oxidationstilstand på -3. Dette skyldes, at brint har en oxidationstilstand på +1, og den samlede ladning af ion er +1.
* tendens til at miste elektroner: Nitrogen i ammoniumion kan oxideres til en højere oxidationstilstand, hvilket betyder, at det kan miste elektroner. Dette tab af elektroner er karakteristisk for et reduktionsmiddel.
Eksempel:
I den følgende reaktion fungerer ammoniumion som et reducerende middel:
`` `
NH₄⁺ + 2O₂ → NO₃⁻ + 2H⁺ + H₂O
`` `
Her oxideres nitrogen i ammoniumion (-3-oxidationstilstand) til nitrat (NO₃⁻) med en +5 oxidationstilstand. Dette skyldes, at ammoniumion mister elektroner, som opnås ved ilt i reaktionen.
Key Takeaway:
Et reduktionsmiddel er et stof, der donerer elektroner og bliver oxideret i processen. Da ammoniumion kan miste elektroner og blive oxideret, fungerer det som et reduktionsmiddel.
Sidste artikelHvad mineral krystalliserer ved den højeste temperatur?
Næste artikelHvad er ligningen for kogende vand?
 Varme artikler
Varme artikler
-
 Helikater møder rotaxaner for at skabe løfte om fremtidig sygdomsbehandlingKredit:University of Birmingham En ny tilgang til behandling af kræft og andre sygdomme, der bruger et mekanisk sammenlåst molekyle som en magisk kugle er designet af forskere ved University of Bi
Helikater møder rotaxaner for at skabe løfte om fremtidig sygdomsbehandlingKredit:University of Birmingham En ny tilgang til behandling af kræft og andre sygdomme, der bruger et mekanisk sammenlåst molekyle som en magisk kugle er designet af forskere ved University of Bi -
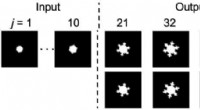 Ny strategi sætter udviklingen af mikroskopiske strukturer i gangIngeniører ved Rice University og Lawrence Livermore National Laboratory bruger neurale netværk til at fremskynde forudsigelsen af, hvordan mikrostrukturer af materialer udvikler sig. Dette eksempel f
Ny strategi sætter udviklingen af mikroskopiske strukturer i gangIngeniører ved Rice University og Lawrence Livermore National Laboratory bruger neurale netværk til at fremskynde forudsigelsen af, hvordan mikrostrukturer af materialer udvikler sig. Dette eksempel f -
 Et biobrændstof til automatiseret varmeproduktionArkadievsky tørv i Tomsk Oblast i Sibirien, Rusland. Kredit:Tomsk Polytekniske Universitet Pyrolyse, en proces med nedbrydning af biomasse, kan organiseres automatisk. Specifikt, det er tilstrække
Et biobrændstof til automatiseret varmeproduktionArkadievsky tørv i Tomsk Oblast i Sibirien, Rusland. Kredit:Tomsk Polytekniske Universitet Pyrolyse, en proces med nedbrydning af biomasse, kan organiseres automatisk. Specifikt, det er tilstrække -
 Enhed forvandler skaller af havdyr til kraft til medicinsk, augmented reality, mobiltelefonenhederEt Purdue-team er ved at omdanne rejeskalmateriale til en funktionel enhed til at generere elektricitet. Kredit:Purdue University En innovation, der bruger materiale, der stammer fra skaller fra k
Enhed forvandler skaller af havdyr til kraft til medicinsk, augmented reality, mobiltelefonenhederEt Purdue-team er ved at omdanne rejeskalmateriale til en funktionel enhed til at generere elektricitet. Kredit:Purdue University En innovation, der bruger materiale, der stammer fra skaller fra k
- Hvad er forholdet mellem tilsyneladende størrelse og lysstyrke af et himmelsk objekt?
- Oversvømmelsesprojekter for skole
- Hvilke to kategorier bruges til at klassificere partikler?
- En halv grad gør en stor forskel i en opvarmende verden
- Hvad sker der, når et bevægende objekt med momentum kolliderer?
- Hvad er miljøproblemer i tempererede buske?


